-
中药红花(Carthami Flos)是菊科植物红花(Carthamus tinctorius L.)的干燥花,传统本草学著作《本草纲目》记载,红花具有活血散瘀,通经止痛的功效[1],其药材和制剂在临床上被广泛用于心脑血管疾病的预防和治疗。现代药理研究表明,其主要药效物质是以羟基红花黄色素A(hydroxysafflower yellow A,HSYA)为代表的查尔酮类化合物和以菸花苷为代表的黄酮醇类化合物,这些化合物均具有良好的心脑血管损伤保护活性[2-3]。红花药材的产量偏低,每平方千米产量仅为18.0~22.5 t[4],其中特有的HSYA[5]、红花红色素等查尔酮类成分在不同品种间差异较大[6]。由于红花中的查尔酮类成分仅特异性地存在于花冠中[7],加之体外组织培养再生率低[8]等原因,对其功能基因的研究工作一直进展缓慢。特别是对于HSYA等红花特有的有效成分,其生物合成相关的功能基因尚不完全清楚,合成通路也未被完全解析[9]。因此,用现代分子生物学技术手段以提高药效物质的含量,是提高红花品质,节约土地资源、降低制药成本的一条新途径。
短链脱氢酶/还原酶(short-chain dehydrogenases/reductases,SDR)在植物次生代谢物的生物合成中广泛参与各类碳-氧双键,碳-碳双键以及烯酮键的氧化还原催化反应。根据SDRs基因序列的特征结构,SDRs超家族可以被分为5个亚家族[10-14]。最早发现并且进行鉴定的两类主要短链还原酶命名为classical和extend,classical类的SDRs基因拥有长度约为250个氨基酸残基,被称为Extended类的SDRs基因在碳基末端因其含有多余的约100个氨基酸残基而得名。另外3种类型SDRs基因分别被命名为intermediate、complex和divergent。这些类型的SDRs基因基于其结合辅酶类型和结合催化位点的不同进行命名分类。此外,SDRs存在与传统类型不同的含有“rossmann-fold”保守结构域的氧化还原酶结构[15-18]。
黄酮类化合物起源于莽草酸途径和苯丙素生物合成途径,1个香豆酰辅酶A(coumaroyl CoA)和3个丙二酰辅酶A(malonyl CoA)在查尔酮合酶的作用下生成二氢查尔酮,然后经查尔酮异构酶催化为二氢黄酮,进一步在各类还原酶,聚合酶和糖基转移酶的作用下,生成终端次生代谢产物组合[19-21]。红花中所含的主要有效成分HSYA具有查尔酮式结构,本课题组前期研究认为:HSYA从前体物质到合成,中间存在必不可少的氧化还原过程。短链脱氢还原酶家族广泛参与植物体内次生代谢,这一类还原酶都带有相似的折叠结构以及催化位点,已有研究表明,其对苯丙烷代谢途径起重要作用[22-23],但有关红花中还原酶基因相关报道较少[24]。故笔者通过对红花转录组数据库、基因表达谱数据库以及代谢组数据库进行分析,筛选在HSYA生物合成途径的关键还原酶基因,并进行功能验证,以期揭示红花次生代谢成分生物合成途径,为定向调控红花的品质提供科学依据。
-
云南巍山红花品系(ZHH0119),采自海军军医大学药学系温室,经海军军医大学郭美丽教授鉴定为菊科植物红花(Carthamus tinctorius L.)。红花种植条件:温度恒定25 ℃,16 h光照,8 h黑暗。采集相关花与组织后迅速存放于液氮或者−80 ℃冰箱中冷冻。
-
按照Trans ZOL Plant植物总RNA提取试剂盒(北京全式金公司,中国)说明书方法提取红花花冠总RNA,按照Transtart One-Step gDNA Removal and cDNA Synthesis Super Mix逆转录试剂盒(北京全式金公司,中国)说明书方法进行cDNA第一链的合成。cDNA于−20 ℃保存。
-
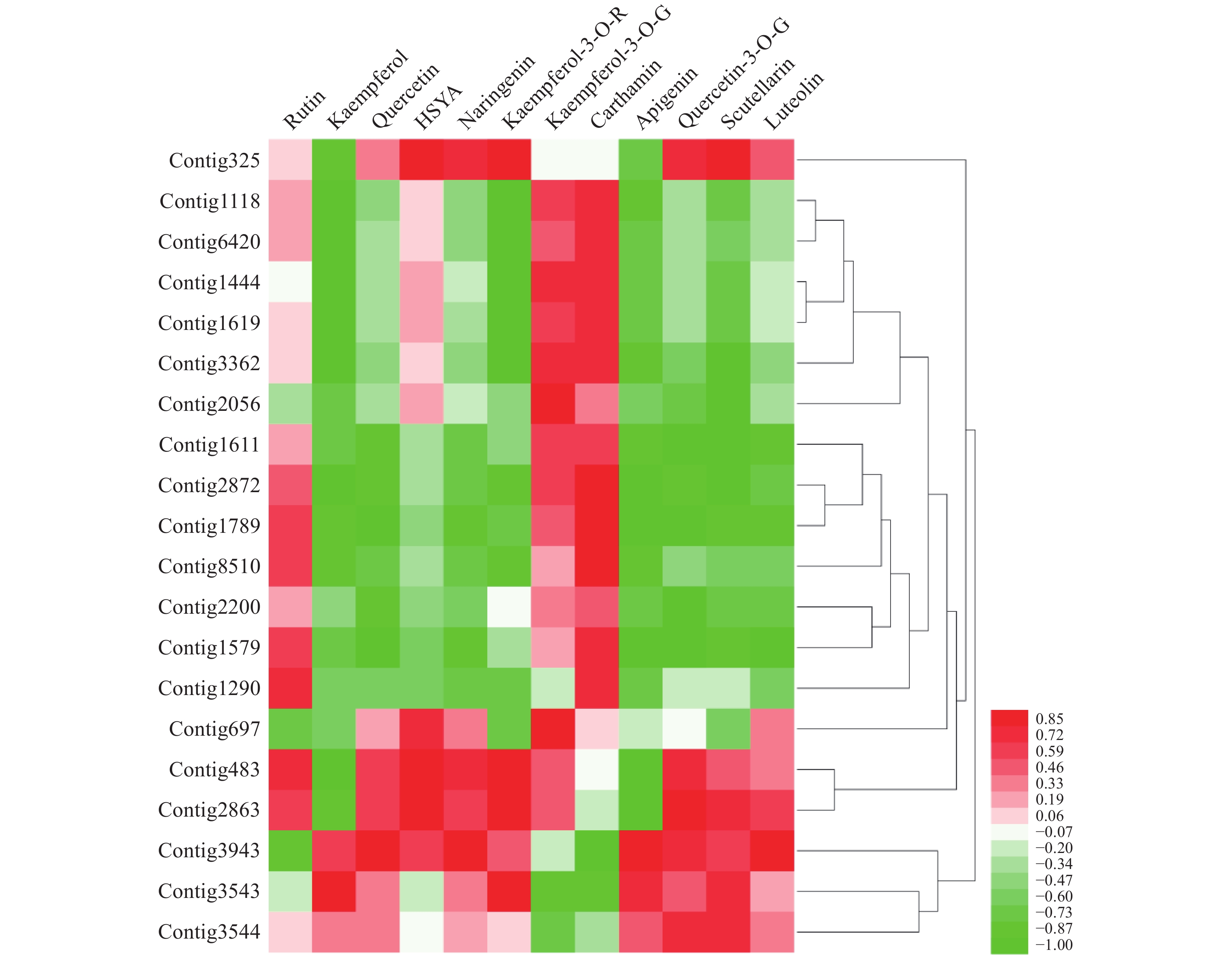
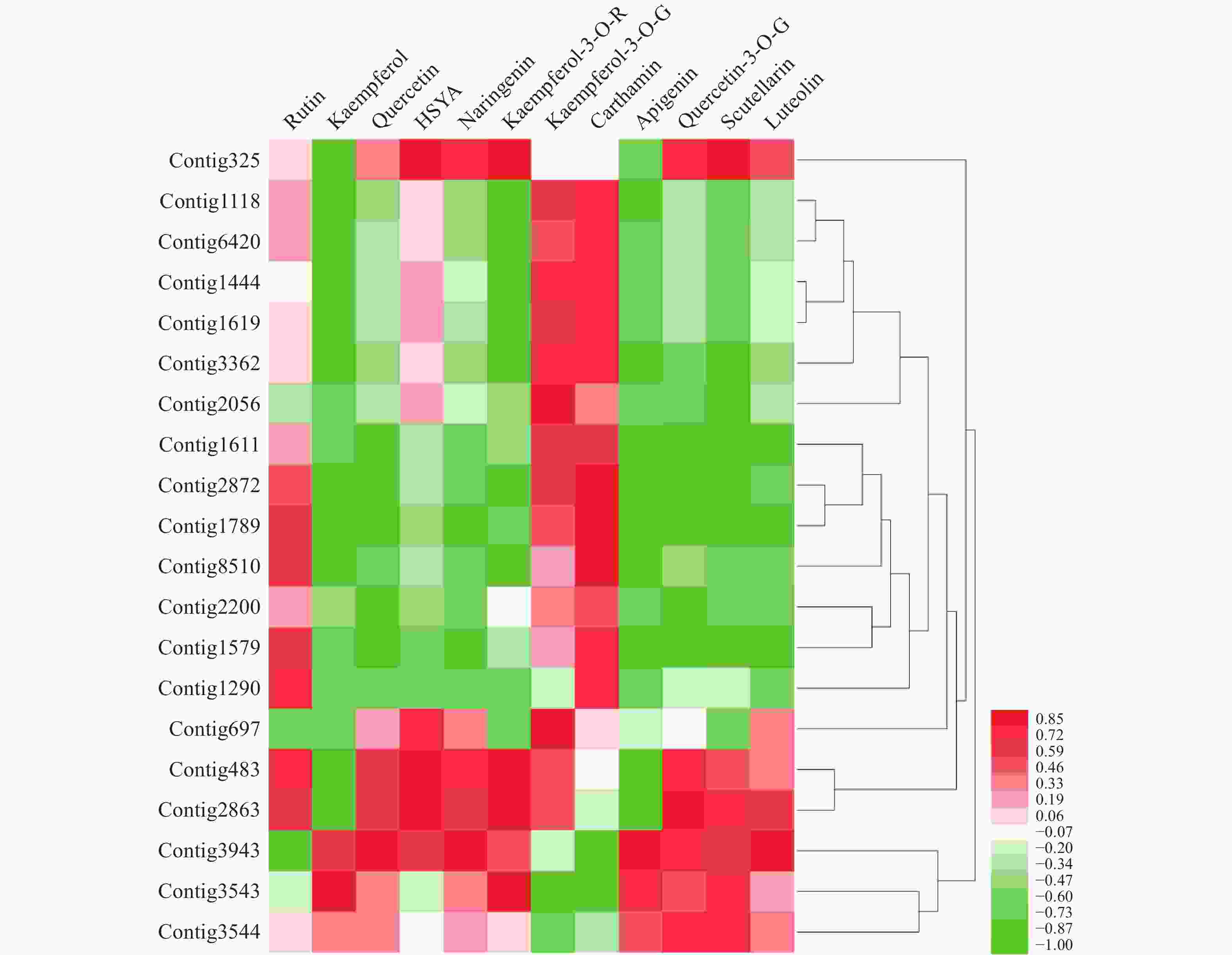
基于数据库中的基因注释以“黄酮还原酶”和“黄酮类化合物生物合成”作为关键词进行检索,筛选出其中可能与HSYA生物合成相关的还原酶基因,将筛选基因不同花期时间的表达量,将其与红花代谢组数据库中同花期的芦丁(rutin)、山柰酚(kaempferol)、槲皮素(quercetin)、HSYA、柚皮素(naringenin)、山柰酚-3-O-芸香糖苷(kaempferol-3-O-rutinoside)、山柰酚-3-O-葡萄糖苷(kaempferol-3-O-gluciside)、Carthamin、芹菜素(apigenin)、黄芩素(scutellarein)、木犀草素(luteolin)、苯丙氨酸(D-phenylalanine) 12个主要成分的含量[12,25]进行皮尔森相关性分析。
-
基于红花花冠EST转录组文库,结合第三代测序技术[26-29]红花花冠全长转录组数据库筛选得到目的基因序列。在其5'端、3'端分别设计特异性引物。按照2× Phanta Flash Master Mix(Dye Plus)高保真酶(南京诺唯赞公司,中国)说明书进行PCR扩增,扩增片段经EasyPure Quick Gel Extraction Kit胶回收试剂盒(北京全式金公司,中国)说明书操作回收后,连接于pEASY-Blunt Zero Cloning Kit(北京全式金公司,中国)载体上,转化至大肠杆菌T1感受态细胞(北京全式金公司,中国)后,涂布在LBA平板上,恒温培养37 ℃过夜,挑取阳性单克隆菌落[30-31],送至上海生工生物有限公司进行菌液测序。
用ExPASyProtParam工具(http://web.expasy.org/compute/)对目的基因的理论等电点(pI),蛋白分子量(MW)和蛋白分子式进行预测。通过Simple Molecule Architecture Research Tool工具(http://smart.embl-heidelberg.de/)对目的基因编码的蛋白质结构功能域进行分析。使用ProtScale(http://us.Expasy.org/cgi-bin/protscale.pl)以及TMHMM(http://www.cbs.dtu.dk/services/TMHMM/)对蛋白质的亲/疏水性和跨膜区域做出预测。使用SignaIP 4.0(http://www.cbs.dtu.dk/services/SignalP/)预测目的蛋白是否含有信号肽。使用NCBI BLAST(https://blast.ncbi.nlm.nih.gov/Blast.cgi)对筛选出的SDRs基因进行BLAST序列比对。通过Neighbor-Joining相邻节点法构建系统发育进化树,自展分析法进行1000次重复[32-34]。使用PBILYON-GRLAND数据库预测构建蛋白质二级结构模型。蛋白三级结构由Protein Homology/analogy Recognition Engine预测。用WOLFPSORT软件(https://wolfpsort.hgc.jp/)进行亚细胞定位预测。
-
取盛花期新鲜红花根、茎、叶、花冠4个部位的新鲜组织和花期Ⅰ(开花前3 d)、花期Ⅱ(开花当天)、花期Ⅲ(开花后1 d)、花期Ⅳ(开花后3 d)4个花期的新鲜花冠,提取总RNA,合成cDNA第一链后,在靠近5'端处对各个基因设计引物,依据Transtart Top Green qPCR super Mix(北京全式金公司,中国)试剂盒推荐体系,以Ct60s(KJ634810)作为内参标记基因,进行qRT-PCR实验,结果使用2−ΔΔCt的方法进行计算分析[35]。
-
根据CtSDR3的开放阅读框和植物真核表达载体pMT-39序列信息,设计无缝克隆引物。以红花cDNA做模板,使用高保真酶进行PCR反应。产物经胶回收后依无缝克隆试剂盒说明书与经NcoI酶切线性化的pMT-39载体进行重组连接。重组载体转化大肠杆菌T1感受态细胞,挑取阳性克隆菌株扩大培养后抽提质粒,提取的pMT39-CtSDR3质粒用冷冻法转至农杆菌GV3101中。LBK+Rif平板筛选阳性克隆后,取1ml OD600 = 0.8的菌液经6 000 r/min,离心3 min后用1 ml 5%蔗糖溶液重悬,加入Silwet-L 1μl,用注射器注射于红花花柱,套袋避光[35]。
在pMT-39的35 s启动子区域设计5'端特异性引物,在目的基因CtSDR3中设计3'端引物。取T2代新鲜叶cDNA第一链作为模板,2× Easy Taq PCR Mix(北京全式金,中国)推荐体系进行PCR反应,确定是否存在目的条带。采集CtSDR3阳性植株花冠以及pMT-39空载体对照植株的花冠,按照上述的qRT-PCR反应体系评价CtSDR3基因的过表达水平,使用UPLC-Q-TOF/MS 检测CtSDR3过表达组和空载体对照组的黄酮代谢物含量,选择以HSYA为代表性成分的8个黄酮类化合物作为检测对象。
-
根据CtSDR3的开放阅读框及蛋白表达载体pGEX-6p-1以及pET-28a序列信息,设计同源重组克隆引物[34]。以红花花冠cDNA为模板,使用高保真酶进行PCR反应。PCR产物经胶回收后依无缝克隆试剂盒说明书与经XhoI、BamHI酶切线性化的载体pGEX-6p-1以及pET-28a进行重组连接。重组载体转化大肠杆菌T1感受态细胞,挑取阳性菌株克隆扩大培养后抽提质粒,提取的重组质粒用热激法转至大肠杆菌Rosseta(DE3)(上海唯地生物,中国)中。
在20 ml LBA液体培养基中培养至OD600为0.6左右,分2份10 ml菌液各加入终浓度为0.3 mmol/L的IPTG和生理盐水。恒温培养箱中16 ℃,100 r/min继续培养16 h[35-36]。菌液离心弃上清液,用1×PBS缓冲液洗涤两次后重悬。超声破碎仪中40 kW,工作时间5 s,循环间隔时间25 s,共15个循环进行破碎[16],裂解完成后取上清与沉淀15 μl,上样检测。
-
通过分析,得到contig325、contig483、contig2863共3个与HSYA具有强相关性的基因(r>0.85),见图1。
-
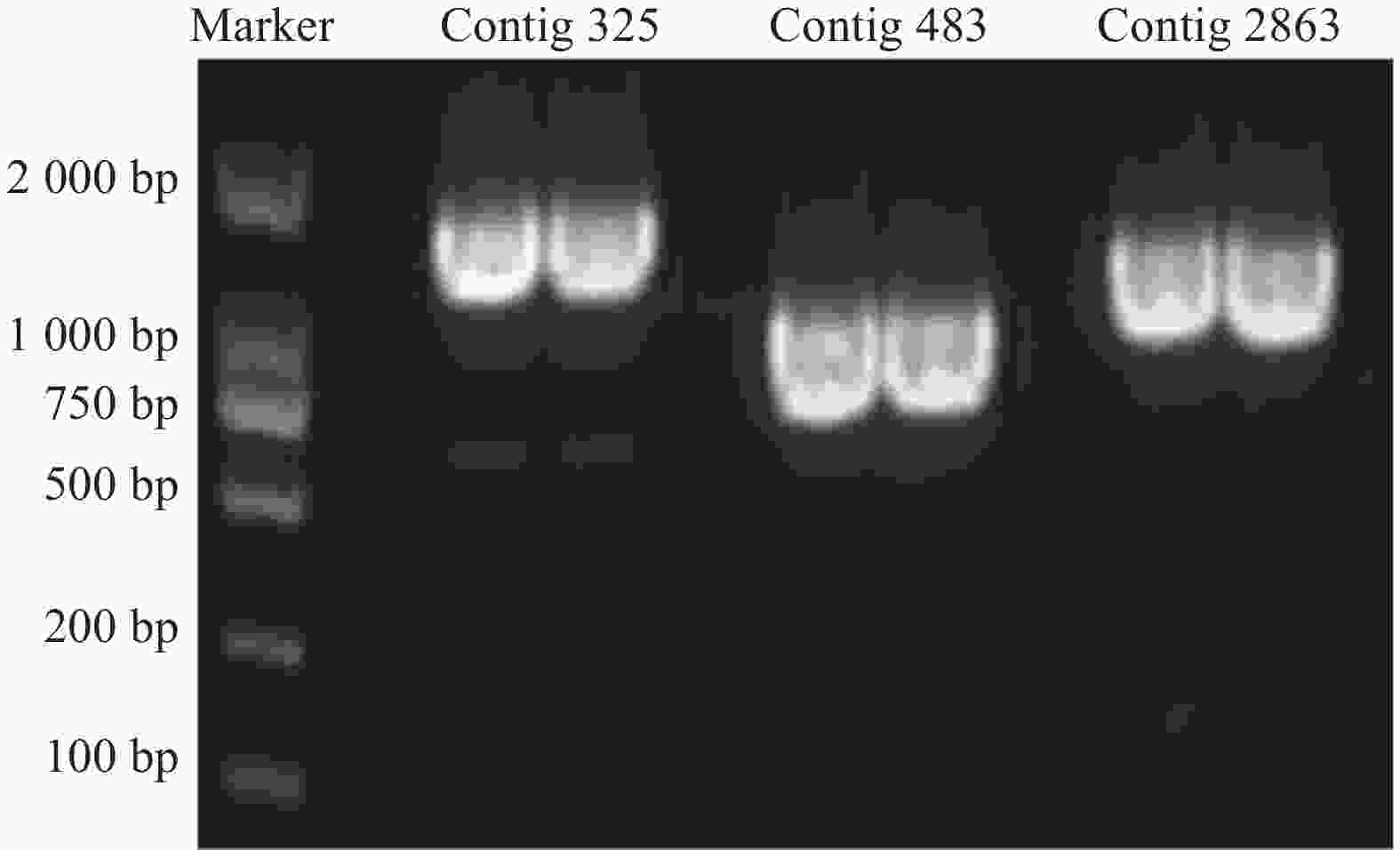
3个目的基因序列信息经测序验证结果如下:contig325全长共1523 bp,开放阅读框1341bp,编码446个氨基酸;contig483全长1393 bp,开放阅读框792 bp,编码263个氨基酸;contig2863全长序列1527 bp,开放阅读框1023 bp,编码340个氨基酸。PCR产物电泳结果如图2所示。
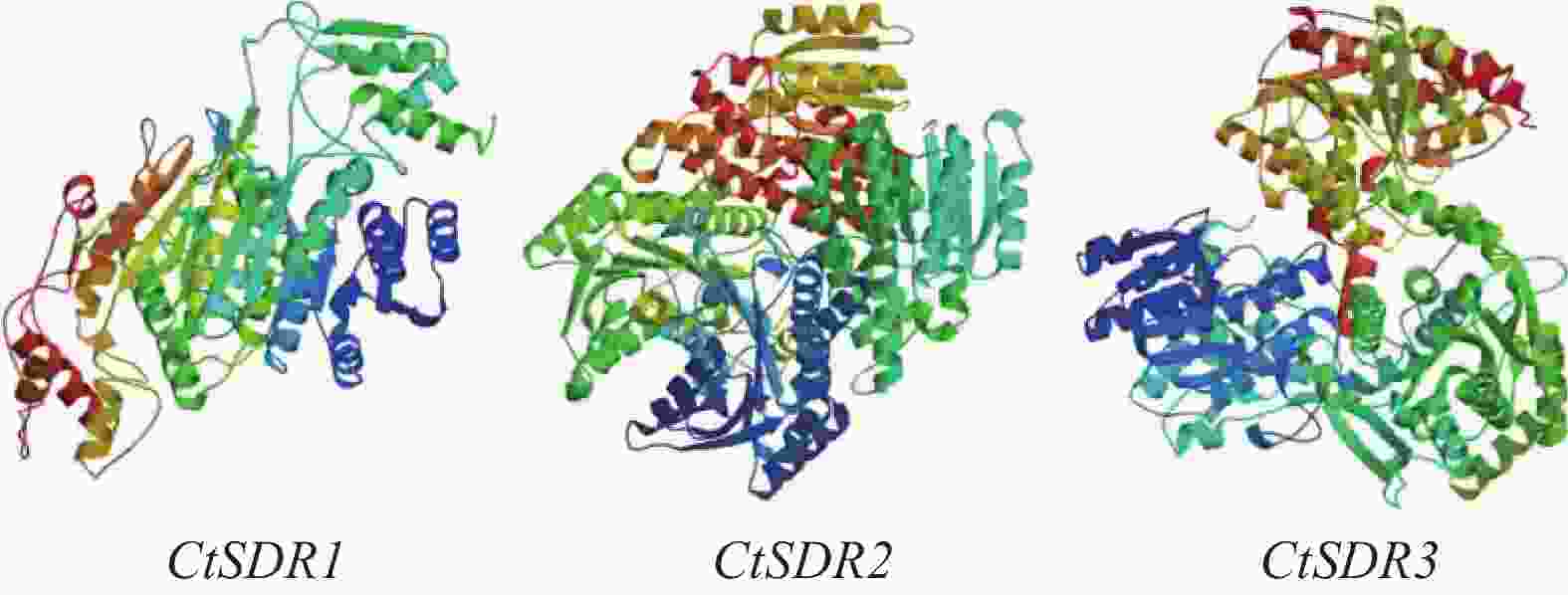
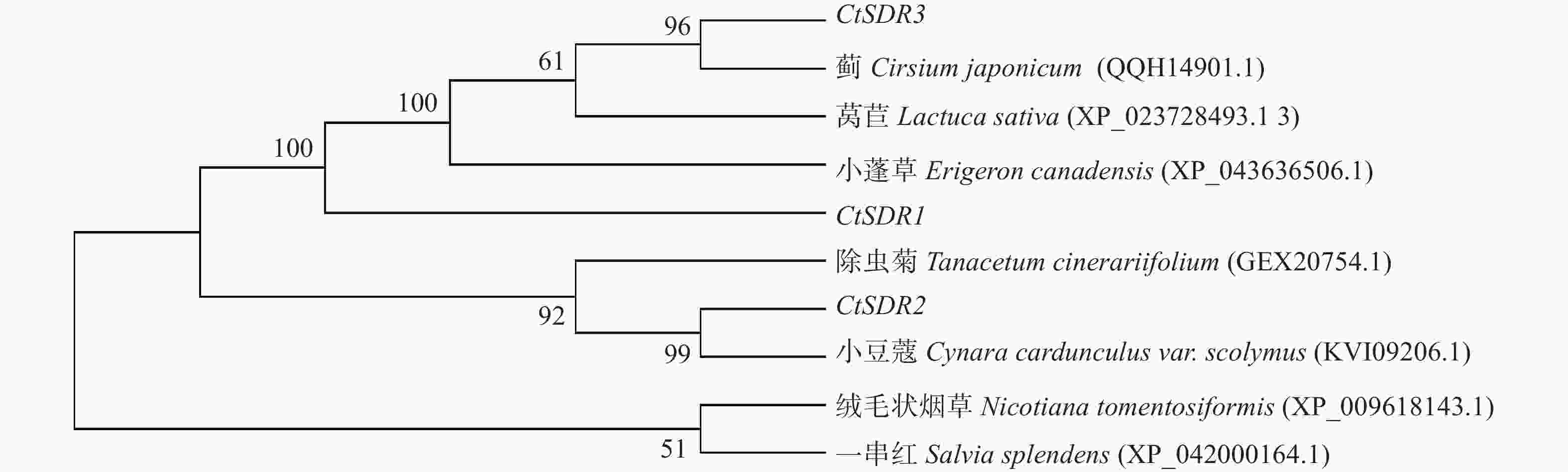
contig325基因编码446个氨基酸,命名为CtSDR1(GenBank登录号:MW792035);Contig483基因编码263个氨基酸,命名为CtSDR2(GenBank登录号:MW792036);Contig2863基因编码339个氨基酸,命名为CtSDR3(GenBank登录号:MW792037)。系统进化树表明CtSDR1与蓟Cirsium japonicum (QQH14901.1)同源性最高;CtSDR2与小蓬草Erigeron canadensis (XP_043636506.1)同源性最高;CtSDR3与小豆蔻Cynara cardunculus var. scolymus (KVI09206.1)同源性最高。Prot-param分析CtSDR1基因所编码的蛋白质分子式C2230H3346N606O639S7,相对分子量为49.2×103,理论等电点pI=9.61;CtSDR2基因所编码的蛋白质分子式C1289H2072N360O379S13,相对分子量为29×103,理论等电点pI=8.63;CtSDR1基因所编码的蛋白质分子式C1691H2614N442O481S9,相对分子量为37.1×103,理论等电点pI=6.80。Prot Scale分析预测CtSDR1、CtSDR2和CtSDR3蛋白为亲水性蛋白,无信号肽属非分泌蛋白。蛋白跨膜性分析显示CtSDR1、CtSDR2和CtSDR3不含有跨膜区域,为非跨膜蛋白。对CtSDR1、CtSDR2和CtSDR3蛋白二级结构的预测显示均属于不规则结构。对CtSDR1、CtSDR2、CtSDR3蛋白质三维结构预测如图3所示。系统进化树如图4所示。亚细胞定位预测显示,CtSDR1、CtSDR2、CtSDR3均可能定位于细胞质。
-
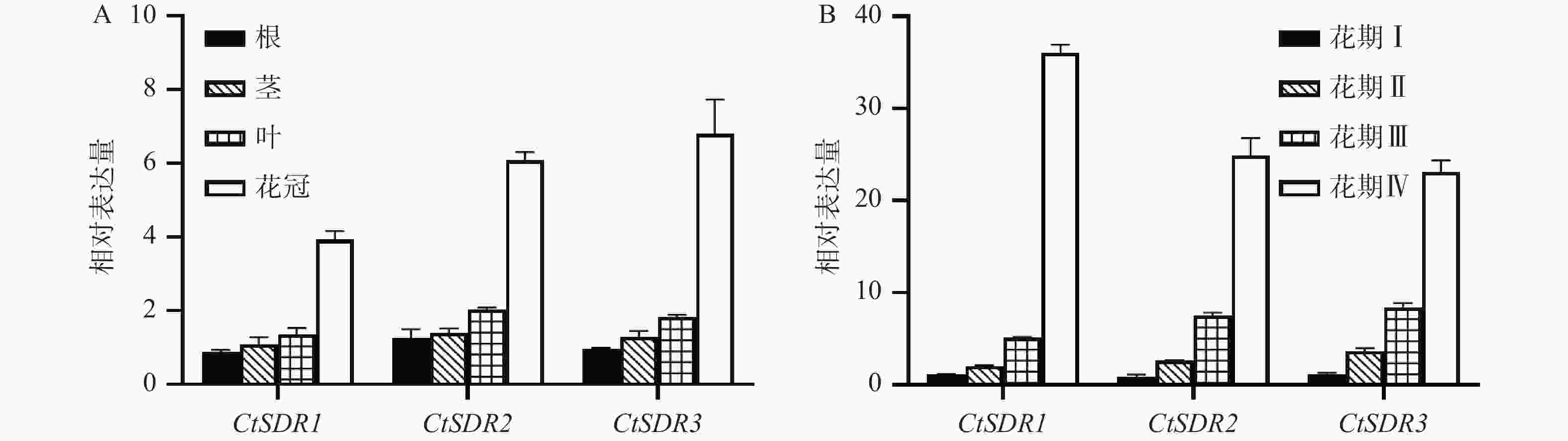
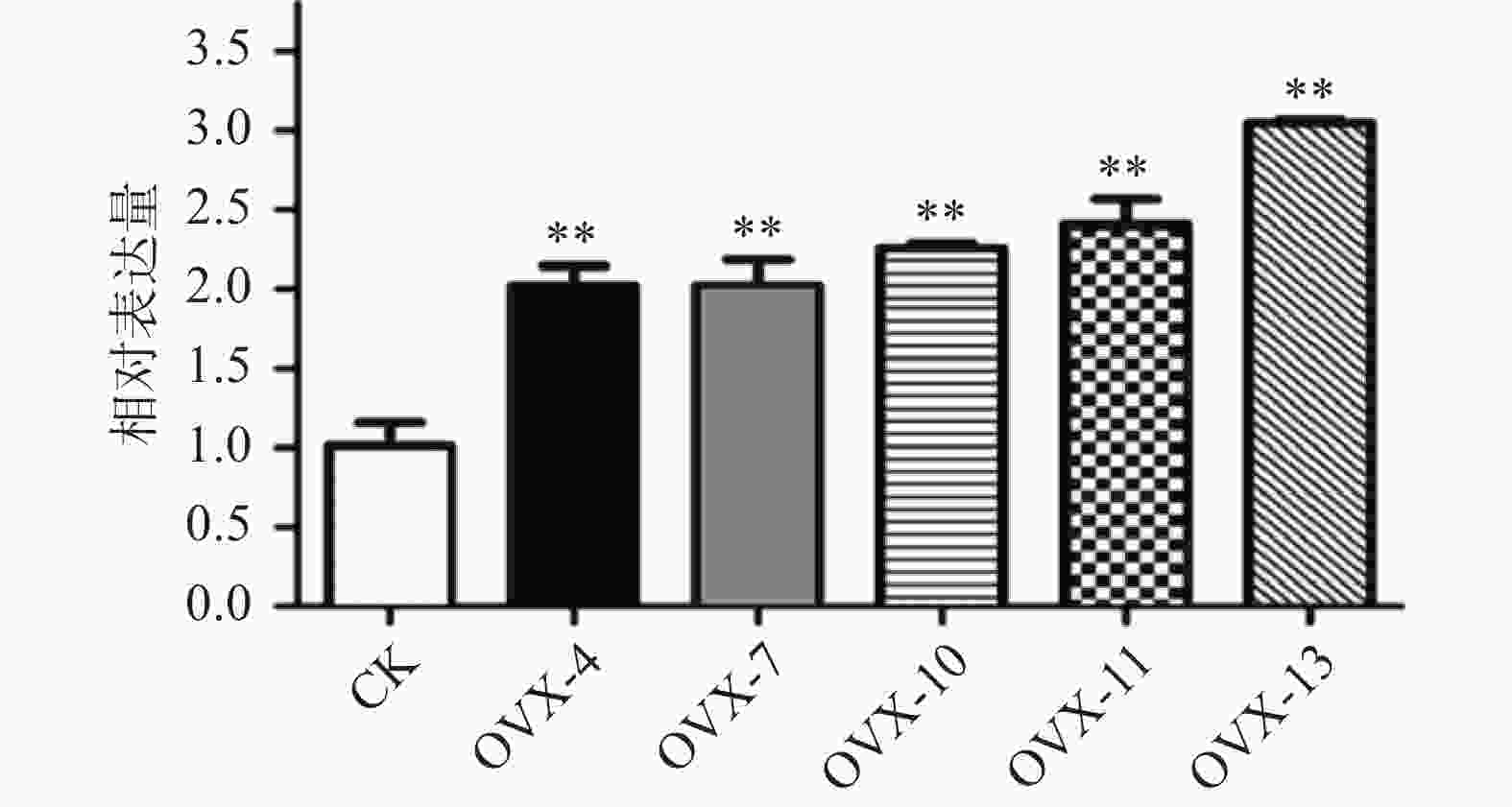
取红花花期的Ⅳ期的红花各个部位进行分析,发现红花花冠内的CtSDR1、CtSDR2、CtSDR3基因表达量从高到低依次均为花冠>叶>茎>根。其中CtSDR1在花冠中的相对表达量约为根中的3倍、而CtSDR2、CtSDR3在花冠中的相对表达量约为根中的4倍。将4个花期的红花花冠进行qRT-PCR分析表明,CtSDR1、CtSDR2、CtSDR3花冠中表达量均随着花冠发育逐渐升高,特别是CtSDR1、CtSDR2、CtSDR3的Ⅳ期花冠对比Ⅲ期花冠的表达量分别提高了7.2倍、2.7倍、2.3倍(图5)。
-
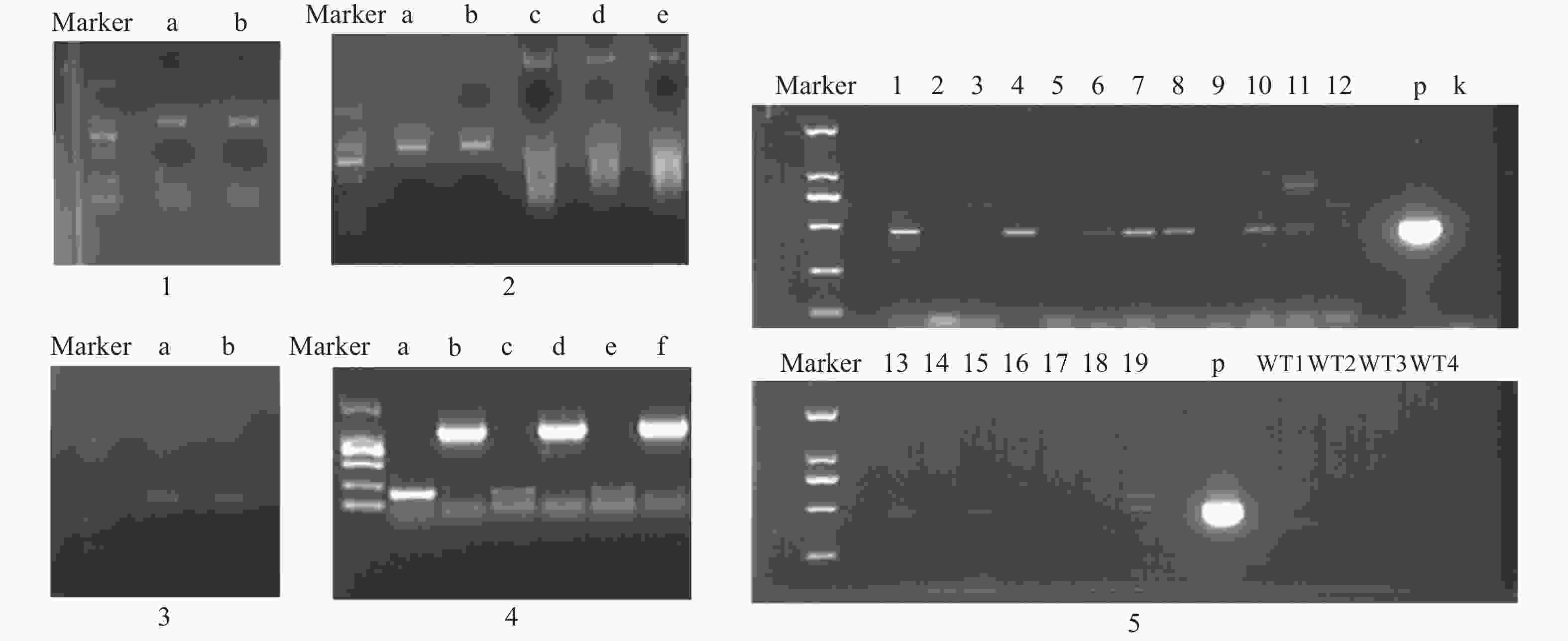
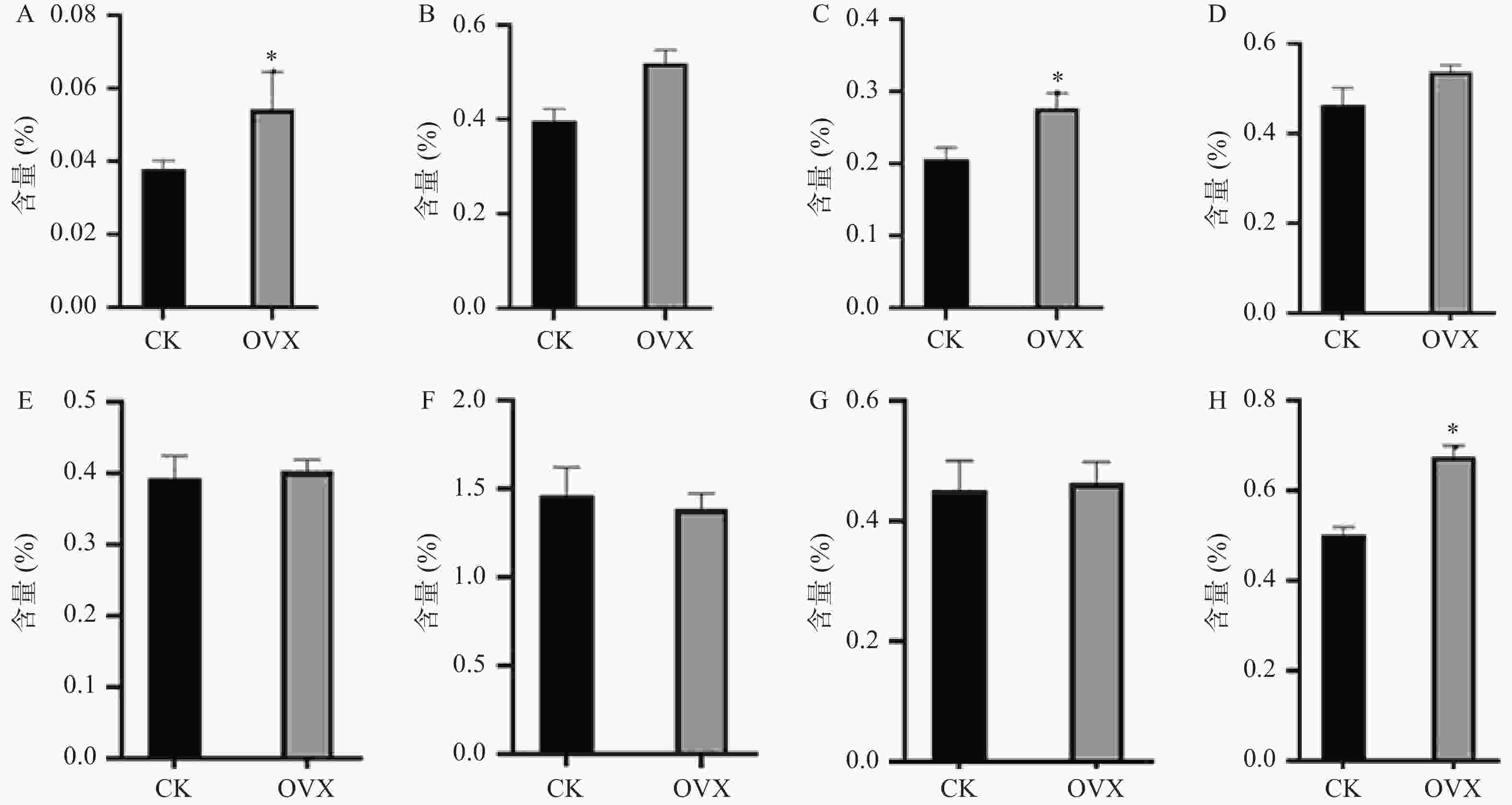
构建真和表达载体并通过PCR鉴定后,我们从19株农杆菌浸染的子代植株中得到5株pMT39-CtSDR3阳性红花植株(图6)。通过qPCR对其CtSDR3基因转录水平进行测定,结果发现阳性红花植株中CtSDR3基因的转录水平得到显著增加,约为空白组株系的2~3倍,CtSDR3的在花冠部位的高表达也证明了研究成功获取CtSDR3过表达红花植株(图7)。通过UPLC-QTOF/MS技术测定阳性转基因红花株系组和空白对照组的目标化合物含量,包括7个红花花冠主要黄酮类化合物及苯丙烷类代谢途径上游关键物质苯丙氨酸(图8),分别为:野黄芩素(scutellarein)、Carthamin、HSYA、山柰酚(kaempferol)、山柰酚-3-O-β-D-葡萄糖苷(kaempferol-3-O-β-D-glucoside)、山柰酚-3-O-β-D-芸香糖苷(kaempferol-3-O-β-rutinoside)、芦丁(rutin)和苯丙氨酸(D-Phenylalanine)。由图8可知,与空白组相比,CtSDR3过表达株系相较于空白组野黄芩素提高了3.6%~9.8%,HSYA提高了7.1%~16.6%,以及苯丙氨酸含量提高了5.5%~15.7%,具有显著性升高。其他化合物含量则有无显著性变化趋势。通过对过表达株系与空白组的含量分析,我们认为CtSDR3基因过表达会引起红花中黄酮类物质的变化,尤其是HSYA含量升高显著。同时,苯丙氨酸代谢途径属于植物重要的次生代谢途径,过表达组引起苯丙氨酸含量的显著上升,上述指标性成分的变化也进一步说明CtSDR3对红花黄酮类化合物次生代谢途径具有一定的影响,但目前我们尚难以判断CtSDR3红花中影响次生代谢产物积累的明确途径。
-
目的片段成功扩增,将目的条带进行胶回收、纯化。CtSDR1、CtSDR1、CtSDR1构建的pGEX-6p-1、pET-28a原核表达载体均有在大肠杆菌内表达,但是CtSDR1-pGEX-6p-1、 CtSDR2-pGEX-6p-1、CtSDR3-pGEX-6p-1、CtSDR1-pET-28、CtSDR2-pET-28a、CtSDR3-pET-28a表达的目的蛋白均形成包涵体,存在于沉淀中。无法进行下一步大量纯化实验,唯有CtSDR2-pGEX-6p-1诱导表达了存在于上清液的目的蛋白,明显可以在上清液中观察到分子量约为50 000的蛋白条带(图9)。
-
越来越多的红花药理学相关研究表明,红花的主要药效物质包括查尔酮类、黄酮醇类等多种黄酮类化合物,其中,查尔酮类HSYA对脑缺血具有保护作用,并且还能抗脑血栓形成以及抗氧化等。研究HSYA的生物合成分途径,对于HSYA的工业化生产具有重要意义。
本研究借助生物学分子技术、结合代谢组分析测定,筛选出3个参与HSYA生物合成途径的关键短链脱氢还原酶基因CtSDR1、CtSDR2和CtSDR3,这3个基因序列具有高度保守性,在不同器官的表达模式均呈现出花冠>叶>茎>根的特点,而且在花冠中的表达量随花冠发育逐渐升高,表明其很有可能参与红花中HSYA等主要药用成分的积累。进一步研究发现,转CtSDR3过表达T2代阳性植株花冠中CtSDR3基因的转录水平增加了2~3倍,次生代谢物HSYA的含量提高了7.1%~16.6%(P<0.05),验证了我们对CtSDR3在红花体内参与黄酮类化合物生物合成功能的推测。本研究中,体外表达CtSDR3蛋白,得到目的蛋白条带,但由于包涵体等原因,蛋白表达和纯化条件仍需要进一步摸索。下一步,我们将对可能起黄酮类生物合成途径的关键SDRs进行深入的生物学特性特别是酶结合位点的研究,为更好地阐释SDRs的生物学功能、利用分子生物育种技术培育高HSYA含量的红花新品种奠定基础。
Characterization and function of short-chain dehydrogenases/reductases in hydroxysafflower yellow A biosynthesis pathway
-
摘要:
目的 探究参与红花黄酮类生物合成途径特别是羟基红花黄色素A(HSYA)关键短链脱氢还原酶基因(SDRs)的功能。 方法 基于红花转录组数据库以及代谢组数据库,筛选参与HSYA生物合成途径的SDRs,用qRT-PCR法分析表达模式。采用无缝克隆技术构建过表达载体,以农杆菌GV3101介导遗传转化云南巍山红花品系,对转基因T2代植株进行阳性验证,并对花冠SDRs的基因表达量进行分析,UPLC-Q-TOF/MS法测定次生代谢物的含量。 结果 筛选出3个参与HSYA生物合成途径的关键短链脱氢还原酶基因CtSDR1、CtSDR2、CtSDR3,表达量从高到低依次为花冠>叶>茎>根。花冠中表达量随花冠发育逐渐升高。对转基因T2代植株进行阳性验证后的花冠进行qRT-PCR分析发现:与空白对照组相比,转CtSDR3过表达T2代阳性植株花冠中CtSDR3基因的转录水平增加了2~3倍,次生代谢物HSYA的含量提高了7.1%~16.6%(P<0.05)。 结论 CtSDR3可能参与了红花中黄酮类化合物特别是HSYA的生物合成,为阐释CtSDR3在HSYA生物合成途径中的功能提供了数据支撑。 Abstract:Objective To explore the function of short-chain dehydrogenases/reductases (SDRs) in safflower flavonoid, especially hydroxysafflower yellow A (HSYA) biosynthesis. Methods SDRs involved in HSYA biosynthesis pathway were screened based on safflower transcriptome database and metabolome database. The expression pattern was analyzed by qRT-PCR. The overexpression vector was constructed by seamless cloning technology, then genetically transformed to the Yunnan Weishan safflower strain by Agrobacterium gv3101. The transgenic T2 generation plants were positively verified, and the gene expression of corolla SDRs was analyzed. The content of secondary metabolites was assayed by UPLC-Q-TOF/MS. Results Three SDRs genes named CtSDR1, CtSDR2 and CtSDR3 involved in HSYA biosynthesis pathway were screened. Their expression in safflower from high to low was corolla > leaf > stem > root. The expression level in corolla increased gradually with corolla development. qRT-PCR analysis of corolla with positive verification of genome insertion sequence showed that the transcription level of CtSDR3 in corolla of T2 positive plants increased by 2~3 times compared with the blank control group, and the content of secondary metabolite HSYA increased by 7.1%~16.6% (P< 0.05). Conclusion CtSDR3 may be involved in the biosynthesis of flavonoids, especially HSYA, in safflower. It provides the support data for explaining the function of CtSDR3 in HSYA biosynthesis pathway. -
Key words:
- short-chain dehydrogenase reductase /
- hydroxysafflor yellow A /
- safflower
-
图 6 真核表达载体构建及阳性鉴定电泳图
注:1. CtSDR3基因开放阅读框(ORF)区扩增产物电泳图,a、b泳道均为CtSDR3基因ORF区克隆PCR产物;2. 真核表达载体pMT-39载体酶切产物电泳图,a、b泳道为CtSDR3 PCR产物,c泳道为pMT-39载体,d、e泳道为pMT-39线性化载体;3. pMT39-CtSDR3重组载体阳性转化子鉴定电泳图,a、b泳道为阳性转化子菌液PCR产物;4. pMT39-CtSDR3质粒转化农杆菌GV3101,a、c和e泳道为空白对照组,b、d和f泳道为阳性克隆菌液PCR产物;5. 红花pMT39-CtSDR3阳性转化植株鉴定PCR产物电泳图,1~19为待鉴定植株,p为pMT39-CtSDR3质粒,k为空白组,WT为野生型红花植株
-
[1] 郭美丽, 张汉明, 张美玉. 红花本草考证[J]. 中药材, 1996(4):202. [2] TU Y H, XUE Y R, GUO D D, et al. Carthami Flos: a review of its ethnopharmacology, pharmacology and clinical applications[J]. REV BRAS FARMACOGN,2015,25(5):553-566. doi: 10.1016/j.bjp.2015.06.001 [3] WANG Y Q, ZHANG S S, NI H L, et al. Autophagy is involved in the neuroprotective effect of nicotiflorin[J]. J Ethnopharmacol,2021,278:114279. doi: 10.1016/j.jep.2021.114279 [4] 贾鑫磊, 何贝轩, 郭丹丹, 等. 红花花冠伸长相关基因CtXTH1的特征与功能研究[J]. 药学学报, 2019, 54(6):1132-1140. [5] 张戈. 红花的化学成分及品质评价[D]. 上海: 第二军医大学, 2001. [6] 张戈, 郭美丽, 张汉明, 等. 不同种质红花药材的高效液相色谱法指纹图谱研究[J]. 第二军医大学学报, 2006, 27(3):280-283. doi: 10.3321/j.issn:0258-879X.2006.03.012 [7] 丁丽丽, 段陈平, 李芳, 等. 红花不同采收期及不同部位中羟基红花黄色素A及山奈素的含量变化[J]. 沈阳药科大学学报, 2015, 32(1):65-69. [8] 杨捷威, 吴婷婷, 郭美丽. 红花组织培养的研究进展[J]. 药学服务与研究, 2012, 12(1):58-62. [9] HUANG L L, YANG X, SUN P, et al. The first Illumina-based de novo transcriptome sequencing and analysis of safflower flowers[J]. PLoS One,2012,7(6):e38653. doi: 10.1371/journal.pone.0038653 [10] COSGROVE D J. New genes and new biological roles for expansins[J]. Curr Opin Plant Biol,2000,3(1):73-78. doi: 10.1016/S1369-5266(99)00039-4 [11] CHENG H, LI L L, XU F, et al. Expression patterns of an isoflavone reductase-like gene and its possible roles in secondary metabolism in Ginkgo biloba[J]. Plant Cell Rep,2013,32(5):637-650. doi: 10.1007/s00299-013-1397-2 [12] MIN T, KASAHARA H, BEDGAR D L, et al. Crystal structures of pinoresinol-lariciresinol and phenylcoumaran benzylic ether reductases and their relationship to isoflavone reductases[J]. J Biol Chem,2003,278(50):50714-50723. doi: 10.1074/jbc.M308493200 [13] 崔扬, 冯彦辉, 陈众峰, 等. 玉米短链脱氢酶基因IDP2557的克隆及其抗旱功能鉴定[J]. 分子植物育种, 2019, 17(22):7300-7305. [14] 王化冰. 黄瓜短链脱氢酶SDR110C家族的生物信息学分析及CsSDR110C14的遗传转化[D]. 泰安: 山东农业大学, 2014. [15] BRAY J E, MARSDEN B D, OPPERMANN U. The human short-chain dehydrogenase/reductase (SDR) superfamily: a bioinformatics summary[J]. Chem Biol Interact,2009,178(1-3):99-109. doi: 10.1016/j.cbi.2008.10.058 [16] JÖRNVALL H, HEDLUND J, BERGMAN T, et al. Superfamilies SDR and MDR: from early ancestry to present forms. Emergence of three lines, a Zn-metalloenzyme, and distinct variabilities[J]. Biochem Bioph Res Commun,2010,396(1):125-130. doi: 10.1016/j.bbrc.2010.03.094 [17] KALLBERG Y, OPPERMANN U, PERSSON B. Classification of the short-chain dehydrogenase/reductase superfamily using hidden Markov models[J]. FEBS Journal,2010,277(10):2375-2386. doi: 10.1111/j.1742-4658.2010.07656.x [18] OPPERMANN U, FILLING C, HULT M, et al. Short-chain dehydrogenases/reductases (SDR): the 2002 update[J]. Chemico-Biological Interactions,2003,143-144:247-253. doi: 10.1016/S0009-2797(02)00164-3 [19] WU Y, WANG Y, MI X F, et al. The QTL GNP1 encodes GA20ox1, which increases grain number and yield by increasing cytokinin activity in rice panicle meristems[J]. PLoS Genet,2016,12(10):e1006386. doi: 10.1371/journal.pgen.1006386 [20] GUO T, CHEN K, DONG N Q, et al. GRAIN SIZE AND NUMBER1 negatively regulates the OsMKKK10-OsMKK4-OsMPK6 cascade to coordinate the trade-off between grain number per panicle and grain size in rice[J]. Plant Cell,2018,30(4):871-888. doi: 10.1105/tpc.17.00959 [21] 靳甜甜. 植物次生代谢途径中黄酮类化合物的生物合成研究[D]. 保定: 河北农业大学, 2014. [22] LEE J, BURNS T H, LIGHT G, et al. Xyloglucan endotransglycosylase/hydrolase genes in cotton and their role in fiber elongation[J]. Planta,2010,232(5):1191-1205. doi: 10.1007/s00425-010-1246-2 [23] SHAO M Y, WANG X D, NI M, et al. Regulation of cotton fiber elongation by xyloglucan endotransglycosylase/hydrolase genes[J]. Genet Mol Res,2011,10(4):3771-3782. doi: 10.4238/2011.October.27.1 [24] 谭政委, 鲁丹丹, 李磊, 等. 红花二氢黄酮醇4-还原酶基因CtDFR1的克隆与分析[J]. 分子植物育种, 2021:1-12. [25] XU F, DENG G, CHENG S, et al. Molecular cloning, characterization and expression of the phenylalanine ammonia-lyase gene from Juglans regia[J]. Molecules,2012,17(7):7810-7823. doi: 10.3390/molecules17077810 [26] SHOJI T, WINZ R, IWASE T, et al. Expression patterns of two tobacco isoflavone reductase-like genes and their possible roles in secondary metabolism in tobacco[J]. Plant Mol Biol,2002,50(3):427-440. doi: 10.1023/A:1019867732278 [27] 朱惠, 杨丽涛, 李杨瑞. 基于三代测序技术的转录组学研究[J]. 生物技术报, 2014(11):130-137. [28] PETIT P, GRANIER T, D'ESTAINTOT B L, et al. Crystal structure of grape dihydroflavonol 4-reductase, a key enzyme in flavonoid biosynthesis[J]. J Mol Biol,2007,368(5):1345-1357. doi: 10.1016/j.jmb.2007.02.088 [29] O'REILLY C, SHEPHERD N S, PEREIRA A, et al. Molecular cloning of the a1 locus of Zea mays using the transposable elements En and Mu1[J]. EMBO J,1985,4(4):877-882. doi: 10.1002/j.1460-2075.1985.tb03713.x [30] 郝爱平. 植物二氢黄酮醇4-还原酶的生物信息学分析[J]. 江苏农业科学, 2014, 42(6):30-34. doi: 10.3969/j.issn.1002-1302.2014.06.009 [31] ISHIDA T, HATTORI S, SANO R, et al. Arabidopsis transparent testa glabra2 is directly regulated by r2r3 myb transcription factors and is involved in regulation of glabra2 transcription in epidermal differentiation[J]. Plant Cell,2007,19(8):2531-2543. doi: 10.1105/tpc.107.052274 [32] ZHANG F, GONZALEZ A, ZHAO M Z, et al. A network of redundant bHLH proteins functions in all TTG1-dependent pathways of Arabidopsis[J]. Development,2003,130(20):4859-4869. doi: 10.1242/dev.00681 [33] 郭丹丹. 红花黄酮类成分生物合成途径关键基因的特征和功能研究[D]. 上海: 海军军医大学, 2019. [34] GRÄFF M, BUCHHOLZ P C F, STOCKINGER P, et al. The Short-chain Dehydrogenase/Reductase Engineering Database (SDRED): a classification and analysis system for a highly diverse enzyme family[J]. Proteins,2019,87(6):443-451. doi: 10.1002/prot.25666 [35] STAVRINIDES A K, TATSIS E C, DANG T T, et al. Discovery of a short-chain dehydrogenase from Catharanthus roseus that produces a new monoterpene indole alkaloid[J]. Chembiochem,2018,19(9):940-948. doi: 10.1002/cbic.201700621 [36] ZHOU Y, ZHANG L, GUI J D, et al. Molecular cloning and characterization of a short-chain dehydrogenase showing activity with volatile compounds isolated from Camellia sinensis[J]. Plant Molecular Biology Reporter,2015,33(2):253-263. doi: 10.1007/s11105-014-0751-z -




 下载:
下载: