-
清肠栓是由上海市名中医马贵同教授创制的医院制剂。该方基于溃疡性结肠炎“湿热瘀互结肠道”的关键病机,以清热化湿、活血止血立法,在锡类散、青黛散治疗黏膜溃疡的基础上优化筛选而来[1-2]。主要由三七和青黛全粉入药,五倍子和马齿苋经提取后浸膏粉入药,再加入冰片、羊毛脂,以半合成脂肪酸酯为基质制备而成的中药栓剂。
冰片为一种传统中药,清香宣散,具有开窍醒神,清热败毒的功效。现代药理学研究表明,冰片具有镇静安神、醒脑、促透、抗菌、抗炎等作用[3]。冰片常被用于肛肠外科,可避免药物的首过效应,提高药物有效性。冰片能开放并透过血脑屏障,有助于其他药物通过血脑屏障,促进疗效[4]。
冰片具有挥发性,龙脑常被作为其主要的质量控制指标,含量测定方法主要包括气相色谱法、衍生化高效液相色谱法、薄层色谱法等[5]。2020年版《中国药典》中,采用气相色谱法测定,冰片含龙脑成分不得少于55.0%,樟脑不得超过0.50%[6]。 目前,已有文献对清肠栓中三七皂苷、人参皂苷、没食子酸、靛蓝和靛玉红进行含量测定[7-8],故本实验采用气相色谱法对清肠栓中冰片含量进行测定,并计算龙脑、异龙脑的相对含量,为进一步提高清肠栓的质量控制提供有效依据。
-
7820A型气相色谱仪、氢火焰离子化检测(FID)(美Agilent 公司);225D-1CN型电子分析天平、BSA124S型电子分析天平(赛多利斯科学仪器有限公司,精度:十万分之一);S450H型超声波清洗器(德国Elma)。
-
清肠栓为院内制剂室提供(批号:210420-210425、211018、211020、211022、211025、190107、190114、190121、190304、190311、190318、190408、190415、190422、190506、190513和200302);樟脑对照品(上海诗丹德标准技术服务有限公司,批号:2814,纯度:95.0%);龙脑对照品(中国食品药品检定研究院,批号:110881-201709,纯度:99.6%);异龙脑对照品(中国食品药品检定研究院,批号:111512-201904,纯度:98.4%);水为超纯水(实验室自制);乙酸乙酯(上海凌峰化学试剂有限公司,分析纯)。
-
采用Agilent7890A型气相色谱仪FID检测器;DIKMA DM-Wax聚乙二醇20000(PEG-20M)毛细管色谱柱(30 m×0.25 mm×0.25 µm);进样口温度为250 ℃;检测器(FID)温度为250 ℃;柱温140 ℃;空气流速为450 ml/min,氢气燃气流速为50 ml/min;尾吹气为25 ml/min;分流比为20:1,进样量为1 µl。理论板数按龙脑峰计算应不低于2 000。
-
称取樟脑对照品适量,精密称定,加乙酸乙酯溶解,制成每1 ml含樟脑0.1 mg的对照品溶液。另取龙脑、异龙脑对照品适量,精密称定,加乙酸乙酯溶解,制成每1 ml含龙脑0.3 mg、异龙脑0.2 mg的混合对照品溶液。
-
取清肠栓(批号:200302)样品10粒,研细,取约60 mg,精密称定,置10 ml量瓶中,加乙酸乙酯8 ml,超声(频率37 kHz,功率800 w)处理30 min,放冷,加乙酸乙酯至刻度,摇匀,滤过,取续滤液,即得。
-
按清肠栓制剂处方比例,配制缺冰片的阴性样品,再按供试品溶液制备方法制备,即得。
-
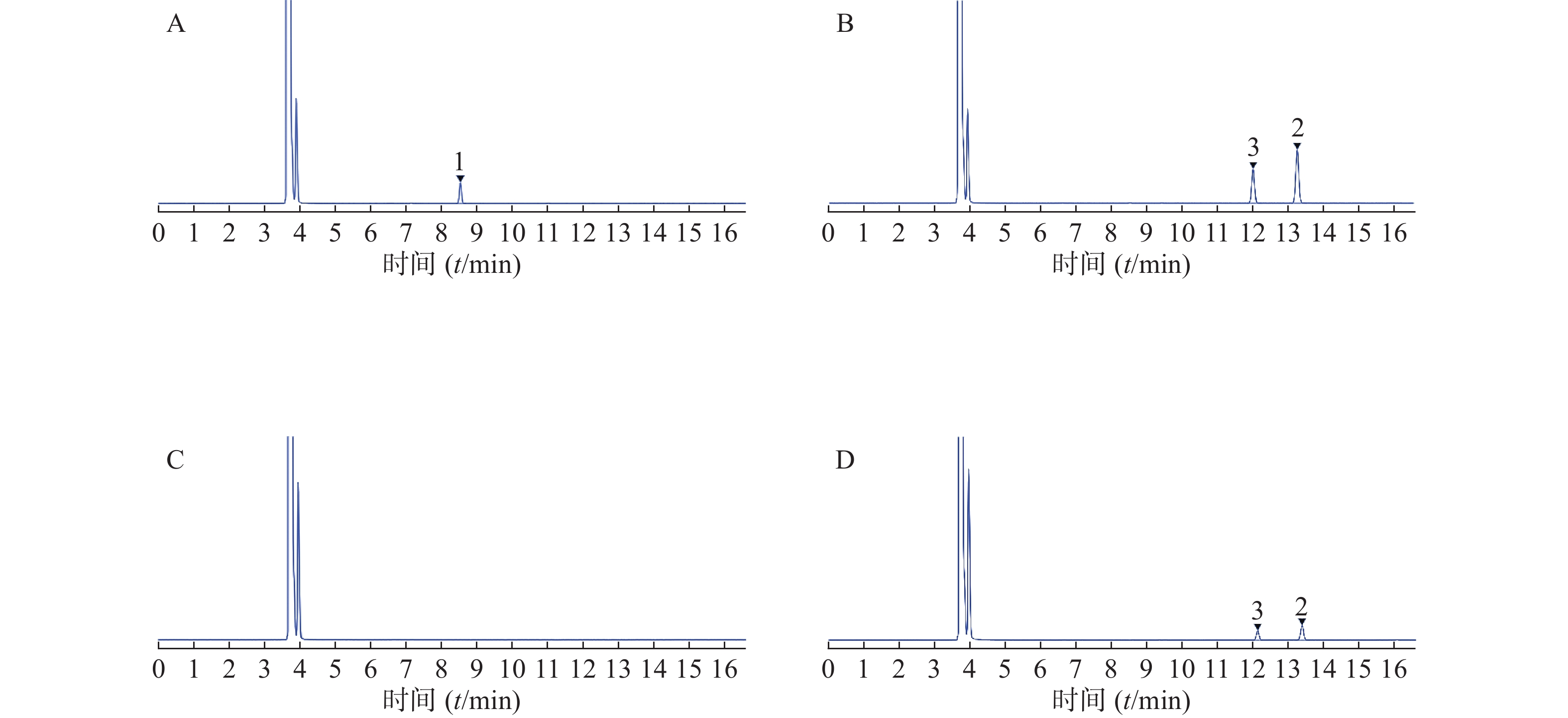
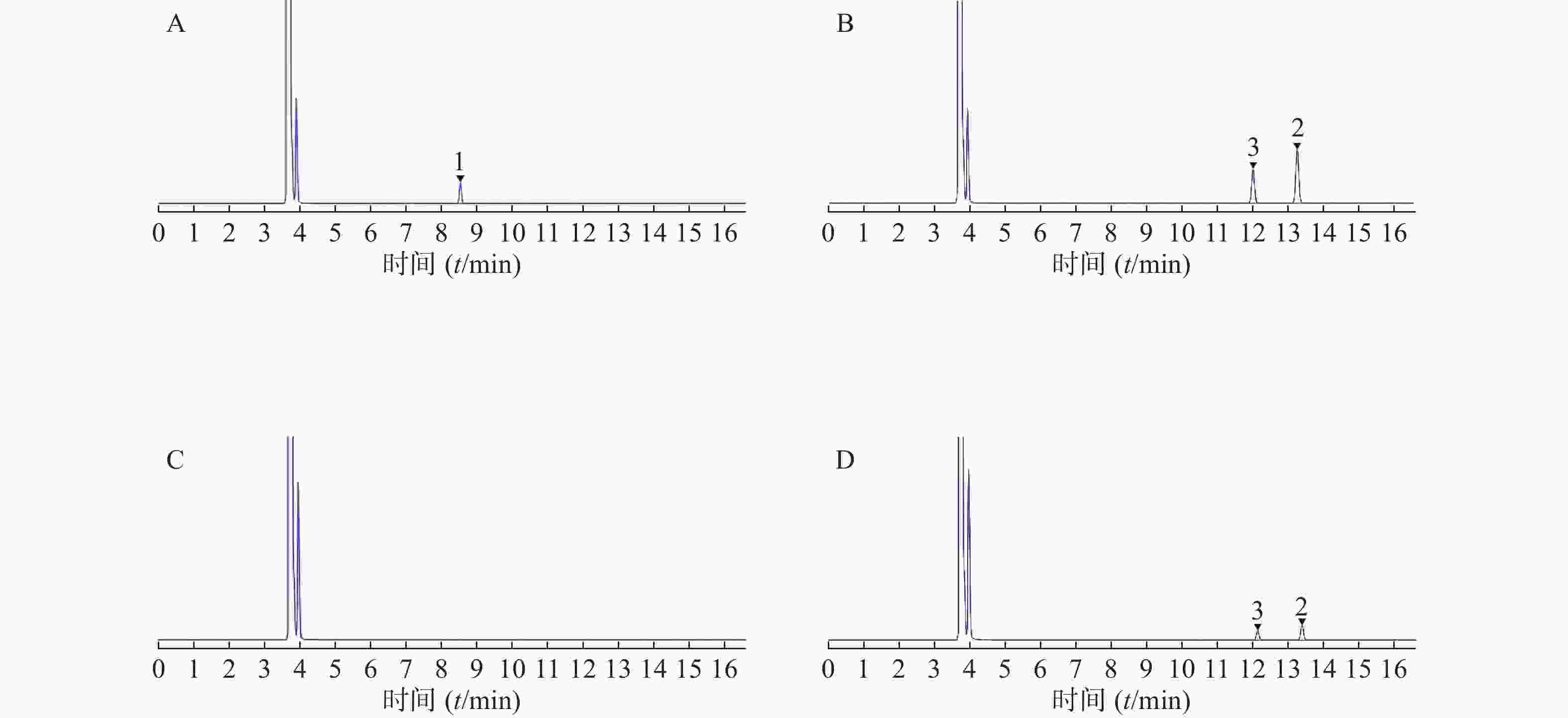
精密吸取樟脑对照品溶液、龙脑和异龙脑对照品溶液、供试品溶液、阴性对照溶液各1 µl,按“2.1”项色谱条件下方法分别进样测定,结果樟脑、异龙脑和龙脑对照品的理论板数分别为88 684、107 331、108 387,远大于规定的2 000。供试品溶液色谱图中,未检出与樟脑对照品溶液保留时间相同的色谱峰,阴性对照溶液色谱图中在与龙脑、异龙脑相同保留时间处无干扰峰,表明该方法专属性良好。色谱图见图1。
-
分别精密称取龙脑对照品14.92 mg、异龙脑对照品10.25 mg、樟脑对照品4.83 mg,置同一10 ml量瓶中,加乙酸乙酯溶解并稀释至刻度,摇匀,制成每1 ml含龙脑1.492 mg、异龙脑1.025 mg、樟脑0.483 mg的混合对照品溶液,作为贮备液。
精密吸取5份贮备液各1 ml,加乙酸乙酯分别稀释50倍、20倍、5倍、2倍、1倍;分别精密吸取5个不同浓度的龙脑、异龙脑、樟脑混合对照品溶液,分别进样1 µl,按按“2.1 色谱条件”项下的方法测定,以进样浓度(X)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线,求得回归方程分别为:Y1=283.4X1+1.320(r=1.000,n=5);Y2=283.5X2+0.8597(r=1.000,n=5);Y3=276.9X3+0.5444(r=1.000,n=5)。线性范围分别为 0.0299~1.497µg、 0.0205~1.025µg、 0.0097~0.4830µg。
-
精密吸取“2.2”项下对照品溶液,按“2.1 ”项的方法测定,重复进样6次,测定峰面积。结果龙脑、异龙脑、樟脑峰面积RSD分别为0.3%、0.4%、0.6%(n=6),表明仪器精密度良好。
-
精密吸取同一供试品溶液(批号:200302),室温下分别放置0、4、8、12、16、20、24 h,按“2.1 色谱条件”项下的方法测定,记录峰面积。结果樟脑未检出,龙脑与异龙脑峰面积的RSD分别为1.6%和1.5%,表明供试品溶液在室温下放置24h稳定。
-
精密称取清肠栓样品粉末60 mg(批号:200302),精密称定,平行称取6份,按“2.3供试品溶液的制备”项下制备供试品溶液,按“2.1”项方法测定,结果均未检出樟脑,龙脑和异龙脑平均含量的RSD分别为0.8%和1.1%(n=6),表明该方法的重复性良好。
-
称取清肠栓样品粉末30 mg(批号:200302),精密称定,平行称取6份,分别精密加入龙脑、异龙脑、樟脑对照品溶液,按“2.3” 项方法制备供试品溶液,按“2.1”项方法测定,记录峰面积,并计算加样回收率。结果见表1。
成分 原有量(mg) 加入量
(mg)测得量
(mg)回收率
(%)平均回收率
(%)RSD
(%)龙脑 0.47 0.50 0.97 100.8 101.0 0.51 0.48 0.50 0.98 101.6 0.47 0.50 0.97 101.2 0.47 0.50 0.97 100.8 0.47 0.50 0.97 100.2 0.47 0.50 0.97 101.4 异龙脑 0.28 0.29 0.58 102.8 102.5 1.66 0.28 0.29 0.59 104.5 0.28 0.29 0.58 104.2 0.28 0.29 0.57 100.4 0.28 0.29 0.58 102.1 0.28 0.29 0.57 100.8 樟脑 0.00 0.13 0.12 97.06 99.69 3.77 0.00 0.13 0.12 93.91 0.00 0.13 0.13 102.6 0.00 0.13 0.13 99.43 0.00 0.13 0.13 104.2 0.00 0.13 0.13 101.0 -
取清肠栓制剂2019、2021年共20个批次的样品,按“2.3”项方法制备供试品溶液,再按“2.1”项方法测定,20个批次均未检出樟脑。样品中龙脑和异龙脑含量见表2(表中1~10为2019年样品,11~20为2021年样品)。
样品序号 龙脑(mg/g) 异龙脑(mg/g) 冰片(mg/g) 1 14.23 8.509 22.74 2 14.19 8.564 22.76 3 14.38 8.665 23.05 4 14.26 8.569 22.83 5 14.28 8.511 22.79 6 14.21 8.571 22.78 7 14.24 8.446 22.68 8 14.41 8.632 23.04 9 14.13 8.329 22.46 10 13.89 8.401 22.29 11 18.76 11.35 30.11 12 18.60 11.20 29.80 13 18.93 11.39 30.32 14 19.03 11.37 30.40 15 18.65 11.26 29.91 16 18.82 11.38 30.19 17 18.89 11.35 30.24 18 18.74 11.28 30.02 19 18.94 11.35 30.29 20 18.88 11.39 30.27 -
乙酸乙酯对冰片具有较好的溶解性,并且样品中其他干扰成分的溶出较少,故选择其作为提取溶剂。本实验考察了不同提取时间(15 min、30 min、45 min)对样品提取效果的影响,观察比较不同条件处理后供试品溶液色谱情况,根据含量结果选择提取时间为30 min。最终以乙酸乙酯为提取溶剂,超声处理30 min作为供试品制备时的提取方式。
-
柱温的选择:由于2020年版《中国药典》中冰片含量测定选择的注温为140 ℃,而查阅文献,部分实验者选择的柱温为160 ℃[9],因此,我们分别选择140 ℃和160 ℃进行试验,根据出峰时间及峰形比较,最终选择140 ℃作为实验条件。色谱柱的选择:实验研究使用的两种色谱柱分别为DIKMA DM-Wax(PEG-20M)毛细管色谱柱(30 m×0.25 mm,0.25 µm);Agilent HP-INNOWAX(PEG-20M)毛细管色谱柱(30 m×0.25 mm,0.25 µm),比较两种色谱柱的塔板数,实验显示色谱峰分离度良好,说明色谱柱对样品的测定结果影响较小,此方法具有普遍性,故最终选择本实验室常用的DIKMA DM-Wax色谱柱。樟脑检出限和定量限确定:检测限及定量限采用信噪比法确认,当信噪比(S/N)为3∶1时,樟脑检出限为1.4 μg/g;当信噪比(S/N)为10∶1时,其定量限为4.6 μg/g。
-
2020年版《中国药典》中,冰片的描述为冰片(合成龙脑),其中对樟脑的检测要求为不得超过0.50%。本次实验,通过查阅文献,参考其它含冰片制剂中对樟脑残留的检测方法[10],对清肠栓样品进行樟脑含量测定,发现成品栓剂中均未检测到樟脑,证明我院制剂室所用冰片符合药典的相关规定。
2020年版《中国药典》是以龙脑作为冰片的含量测定指标,但通过查阅文献可知,近年对冰片的含量测定中,多以龙脑与异龙脑总量来计算冰片的含量,[11-14]。考虑到本次实验是完善清肠栓的内控标准,提高制剂的稳定性,故本实验以龙脑和异龙脑的总量来计算冰片的含量。
综上所述,本方法为冰片中龙脑、异龙脑的含量测定和樟脑限度检查制定提供参考,操作简单、重复性良好、结果准确,可用于清肠栓中冰片的质量控制。
Determination of camphor residue and borneol content in Qingchang Suppository by GC
doi: 10.12206/j.issn.2097-2024.202208110
- Received Date: 2022-08-31
- Rev Recd Date: 2023-03-15
- Available Online: 2023-09-25
- Publish Date: 2023-09-25
-
Key words:
- GC /
- Qingchang Suppository /
- Camphor /
- Borneol /
- Isoborneol /
- Content determination
Abstract:
| Citation: | PAN Yujiong, HE Zhigao, ZHOU Xin, ZHANG Hengzhou, YANG Yuehong, HUANG Jingshan. Determination of camphor residue and borneol content in Qingchang Suppository by GC[J]. Journal of Pharmaceutical Practice and Service, 2023, 41(9): 552-556. doi: 10.12206/j.issn.2097-2024.202208110 |







 DownLoad:
DownLoad: