-
银屑病,俗称牛皮藓,是一种由多种因素造成自身免疫应答紊乱的慢性炎症性皮肤病[1]。该病在欧美国家的发病率在1%~3%,在中国的发病率为0.5%[2]。目前,银屑病的发病机制尚不清楚,普遍认为与遗传、环境和免疫等因素有关[3]。银屑病发病病程长,难以治愈且易复发。根据发病特征可分为多种类型,其中,以斑块状银屑病最为常见[4]。临床常用生物制剂治疗银屑病,具有起效快和疗效更优的特点。近年来,用于治疗银屑病的生物制剂包括有TNF-α抑制剂、IL-12/23抑制剂、IL-17抑制剂和IL-23抑制剂。代表药物有阿达木单抗(adalimumab)、乌司奴单抗(ustekinumab)以及司库奇尤单抗(secukinumab)等[5-6]。这些药物疗效确切,但有对部分患者无效或者长期使用容易出现耐受的问题[7]。bimekizumab(bim)是优时比制药为克服上述问题开发的第一个针对IL-17A和IL-17F的双重抑制剂,2021年8月在获欧盟批准上市。多项临床研究显示,bim治疗银屑病有良好疗效,但国内外没有关于bim治疗斑块状银屑病的循证医学证据,同时探索bim与已经上市的一些药物的疗效对比差异,笔者期望通过系统评价bim治疗中重度斑块状银屑病的疗效与安全性,为临床使用bim提供更多证据与依据。
-
随机对照试验(RCT),中英文不限。
-
临床被诊断为中、重度斑块状银屑病的18岁以上(含18岁)患者[4],患病时间≥6个月,严重程度指数(PASI)评分≥12,银屑病累及体表面积(BSA)≥10%,研究者总体评估评分(IGA)评分≥3。
-
试验组采用bim,对照组采用安慰剂或其他药物治疗。
-
主要结局指标:第12周或者16周患者经治疗后PASI 90和PASI 100的患者例数;次要结局指标:第12周或者16周IGA达0或1的患者例数;安全性指标:第12周或者16周试验组和对照组患者发生的不良事件。
-
非RCT试验;研究对象为非斑块状银屑病的患者;未提供相关的结局指标。
-
在Cochrane Library、Pubmed、MEDLINE、EMBASE、Web of Science、知网、万方、维普、CBM等数据库检索符合标准的文献并手工检索纳入研究的参考文献,检索截止时间为2022年1月30日,语种仅限中英文。英文以bimekizumab、Psoriasis、randomized controlled trial。中文以bimekizumab、银屑病、随机对照试验为检索词。
-
由两位研究者分别对纳入的研究进行题目、摘要阅读,根据纳入和排除标准筛选文献,若有分歧再由第3位评价者来判定。提取内容包括第一作者、发表年份、研究对象例数、干预措施、研究对象年龄、体重、结局指标等信息。
-
两位研究者独自采用Cochrane系统评价员手册5.1.0提供的偏倚风险评估工具对纳入的研究进行质量评价,从随机分配的产生方法、分配隐藏、双盲、结果数据是否完整、是否存在选择性报道及其他可能的偏倚来源等方面进行评价[8]。
-
采用RevMan 5. 3软件对纳入研究进行系统评价,二分类变量采用风险比(RR)或优势比(OR)表示效应量,连续性变量则采用加权均数差(WMD)表示,用95%可信区间(95%CI)进行区间估计。研究间的异质性用P值和I2检验评价,若P<0.05,I2>50% ,表明研究间具有异质性,分析异质性的可能来源,采用随机效应模型。若P>0.05,I2<50%,采用固定效应模型。
-
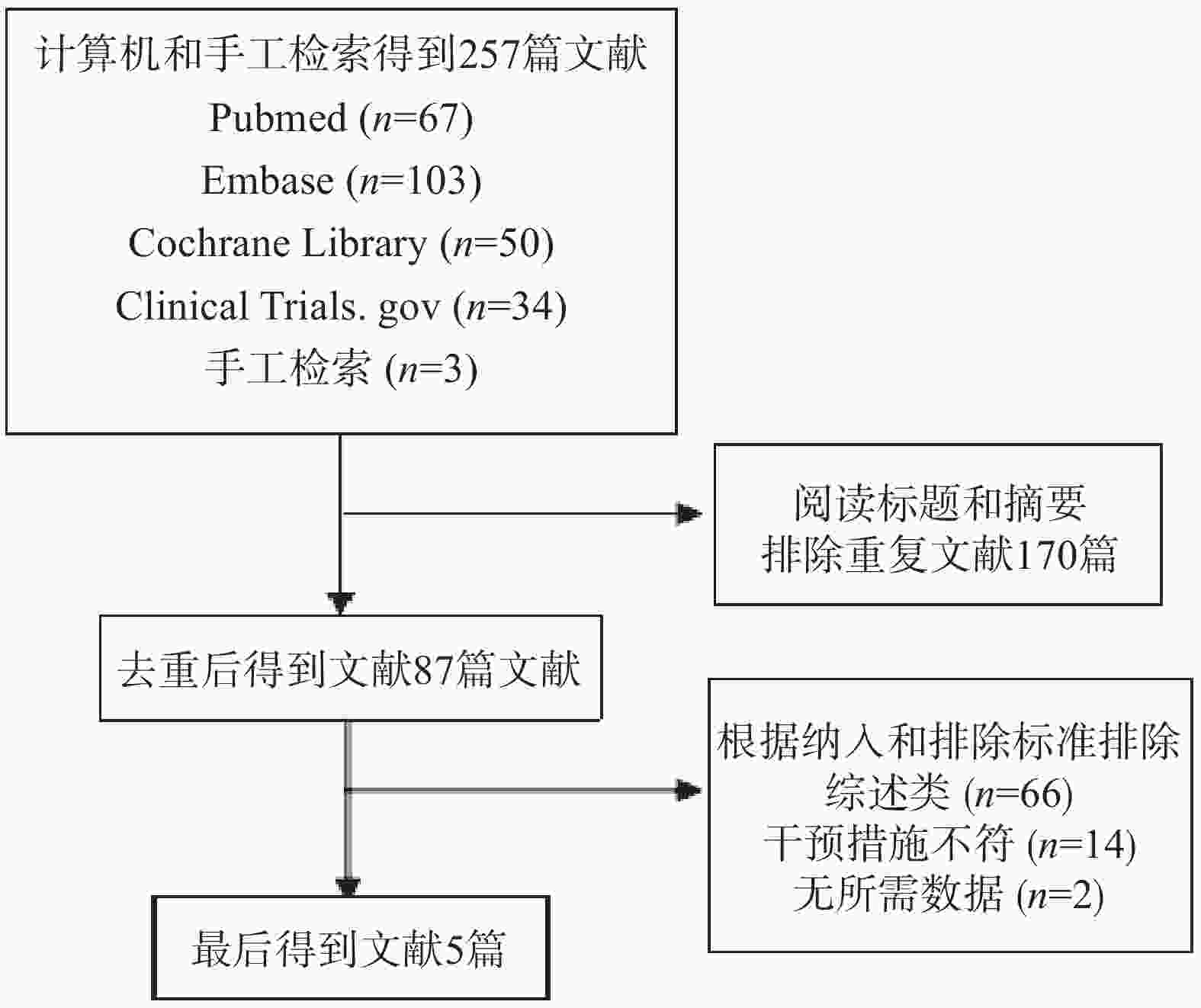
根据检索策略共检索到257篇文献,阅读标题和摘要剔除重复文献后得到得到87篇文献,阅读全文后,根据纳入和排除标准最后得到5篇文献[9-13],其中一篇文献报道了安慰剂和阳性药物两种对照组,按两项试验处理。因此,最终纳入5篇文献,6项研究,一共2308例患者,且6项研究均为RCT,发表语种均为英文,所有纳入研究的基线特征基本相似,文献筛选流程见图1,纳入的文献的基本特征见表1。
研究 例数(n) 干预措施 年龄 体重(m/g) 病程/年 PASI/分 结局指标 Warren RB 2021[9] 319
159bim, 320mg, sc
ada, 40mg, sc45.3±13.2
45.5±14.389.6±21.4
90.5±22.120.4±13.2
16.2±11.920.5±6.9
19.0±5.9PASI90/100 IGA0或1
不良反应Reich K 2021a[10] 321
163bim, 320mg, sc
ust,45mg/90mg, sc45.2±14.0
46.0±13.688.7±23.1
87.2±21.116.0±11.6
17.8±11.622.0±8.6
21.3±8.3PASI90/100 IGA0或1
不良反应Reich K 2021b[10] 321
83bim, 320mg, sc
placebo45.2±14.0
49.7±13.688.7±23.1
89.1±26.416.0±11.6
19.7±13.822.0±8.6
20.1±6.8PASI90/100 IGA0或1
不良反应Papp KA 2018[11] 43
42bim, 320mg, sc
placebo42.5±13.6
46.7±12.386.9±21.7
88.8±21.215.9±9.5
15.0±11.819.4±6.4
18.9±5.8PASI90/100 IGA0或1
不良反应Lebwohl M 2021[12] 373
370bim, 320mg, sc
sec, 300mg, sc45.9±14.2
44.0±14.790.1±21.3
88.8±20.018.4±13.1
17.2±12.320.2±7.5
19.7±6.7PASI90/100 IGA0或1
不良反应Gordon K B 2021[13] 349
86bim, 320mg, sc
placebo44.5±12.9
43.5±13.188.7±20.6
91.7±22.219.6±13.3
19.1±12.820.4±7.6
20.1±7.6PASI90/100 IGA0或1
不良反应注:bim:bimekizumab,ada:阿达木单抗,ust:乌司奴单抗,sec:司库奇尤单抗,placebo:安慰剂,sc: 皮下注射,PASI: 银屑病皮损面积和严重程度指数 -
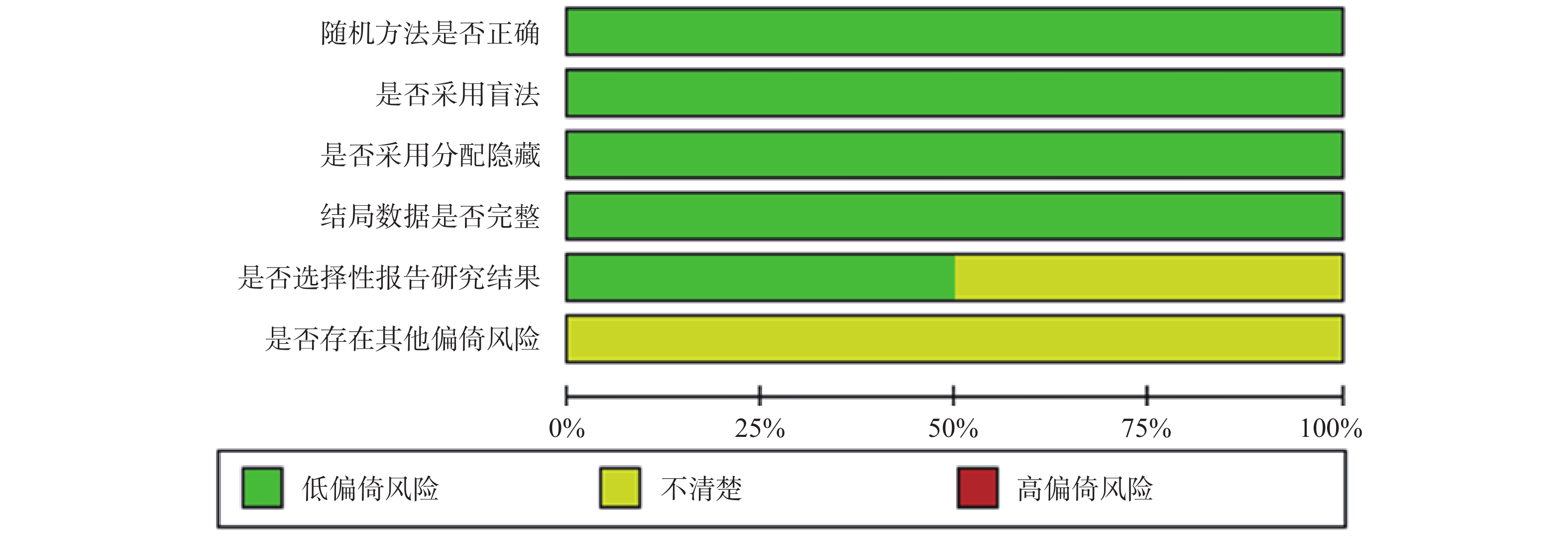
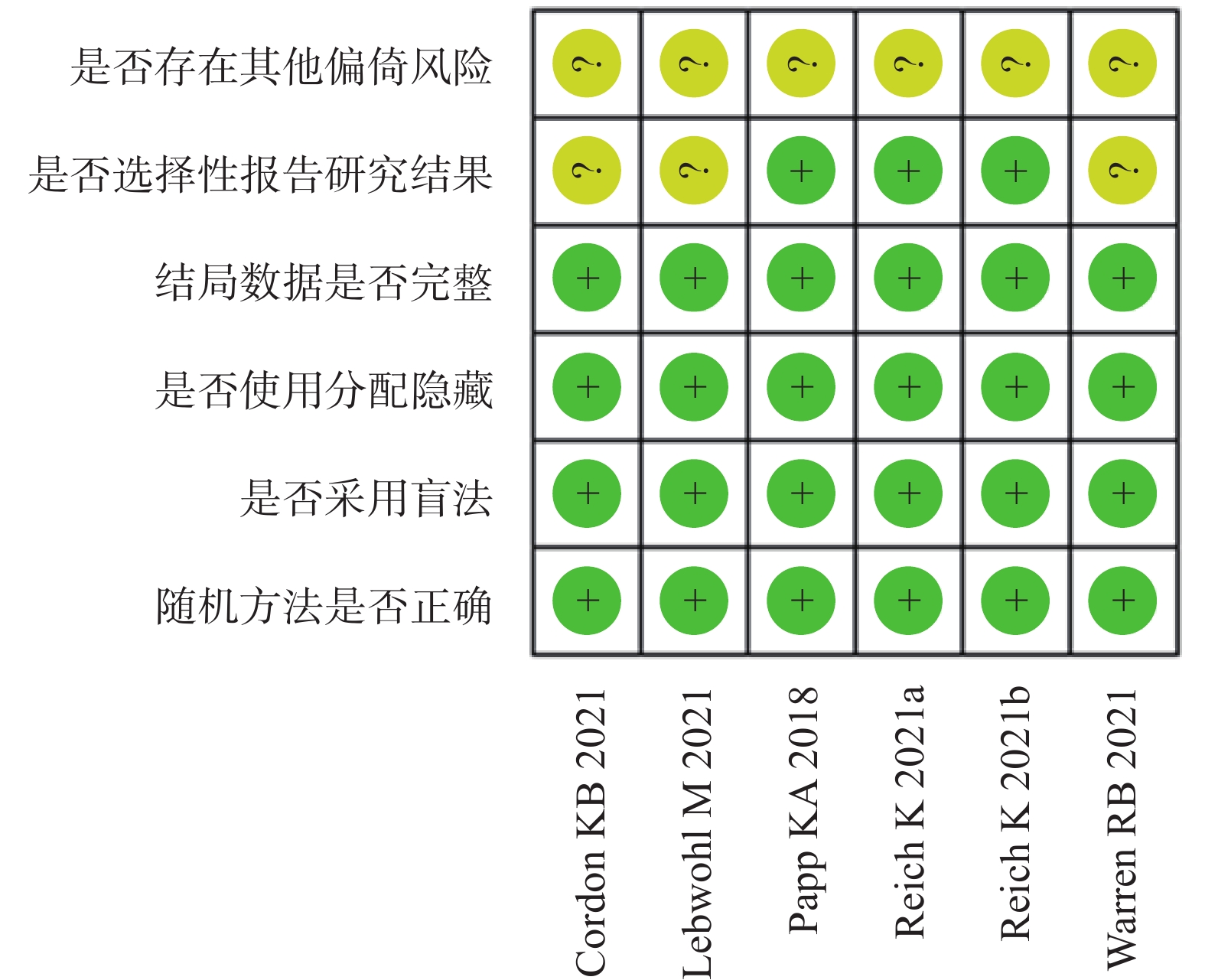
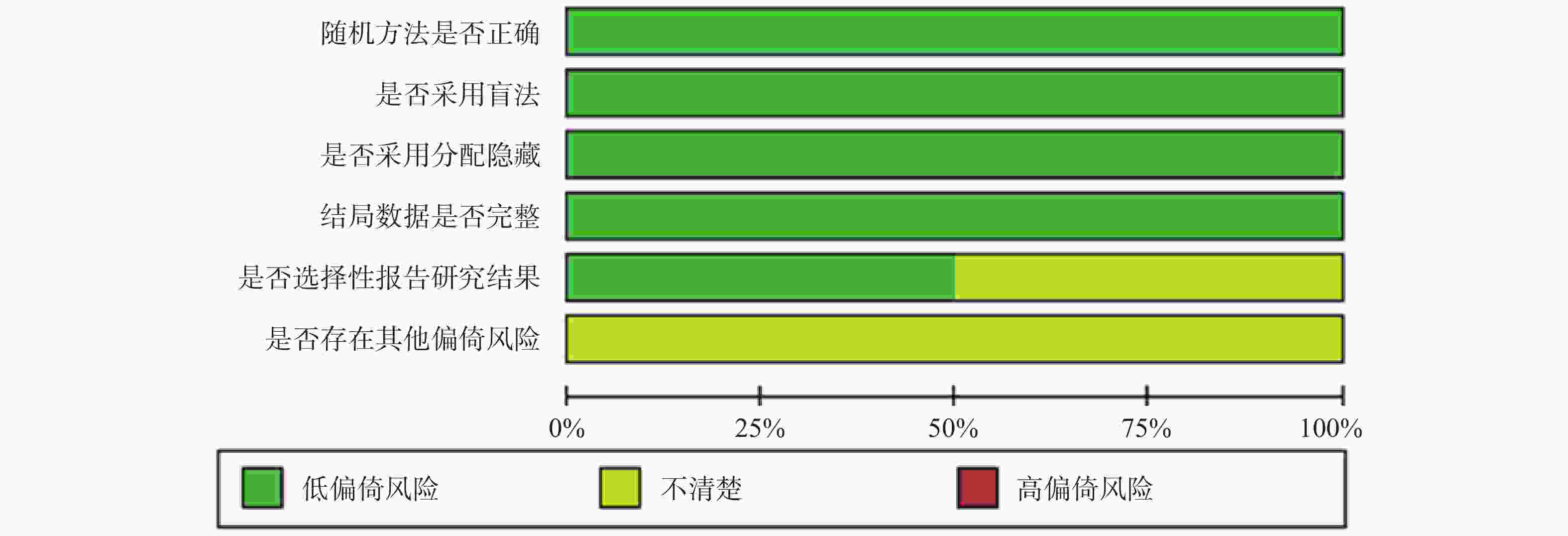
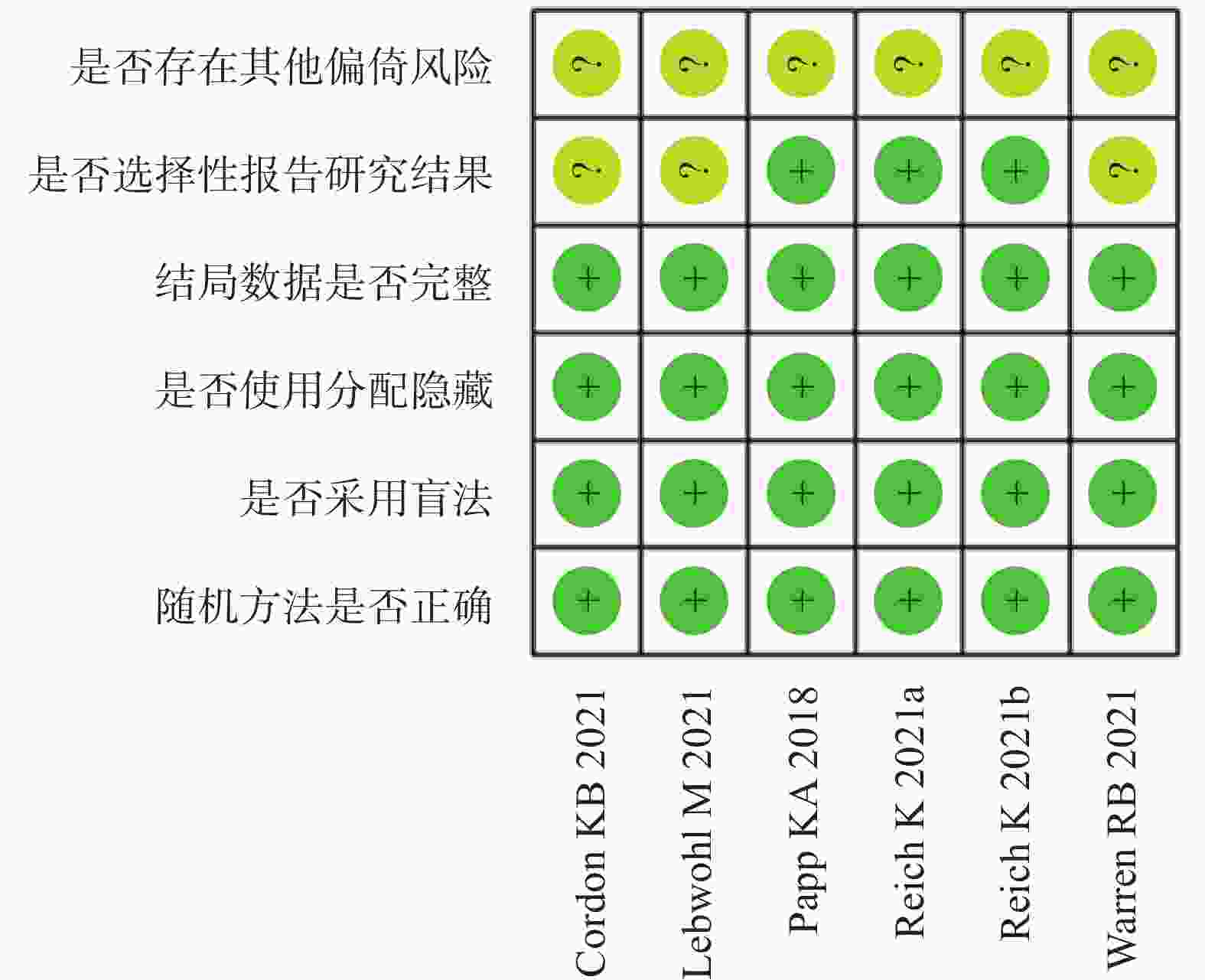
纳入的5[9-13]篇文献,6项研究均报道随机方法是由交互式语音应答系统产生,所有研究都为双盲,结果完整,3项研究未进行选择性报道和所有研究的其他偏倚风险均不清楚,纳入的研究的具体质量评价见表2,偏倚风险评价见图2、图3。
-
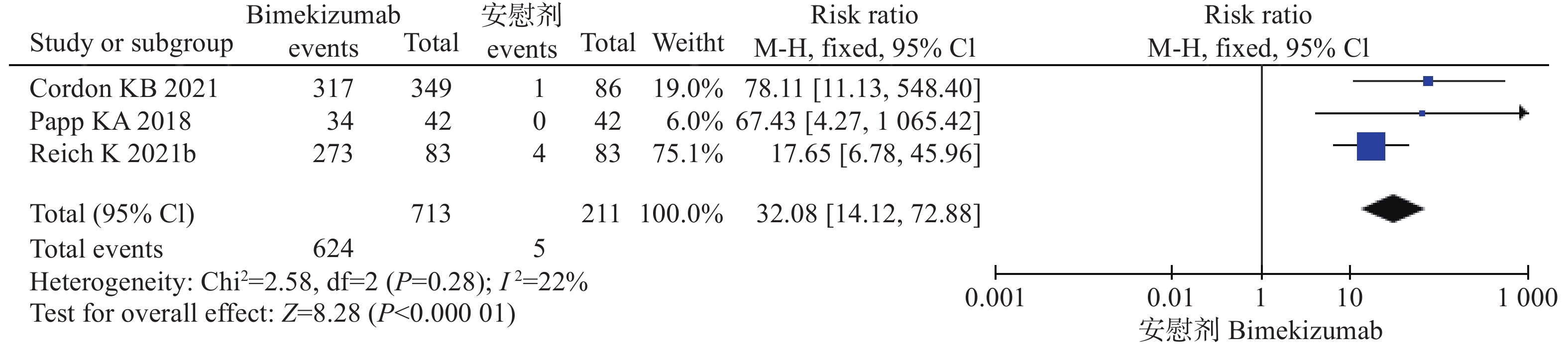
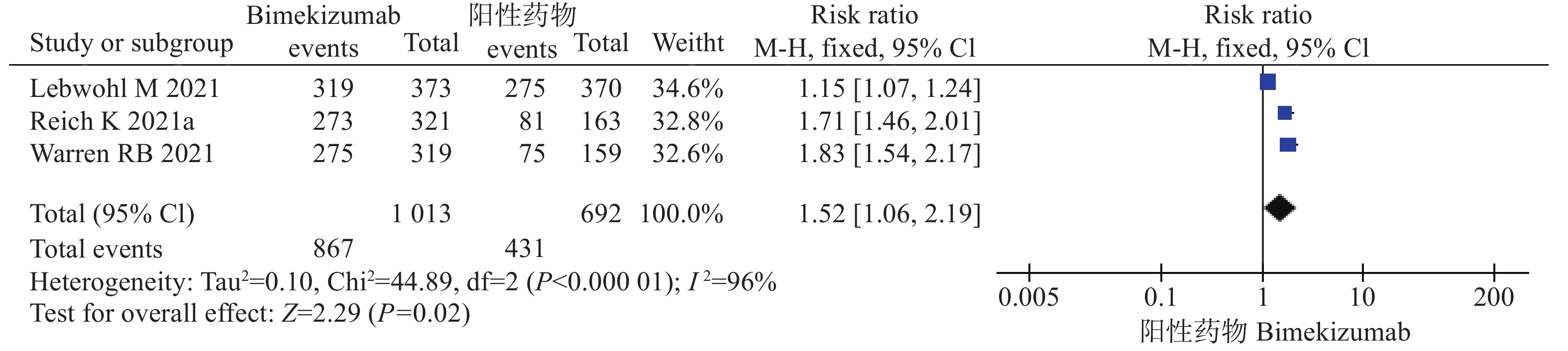
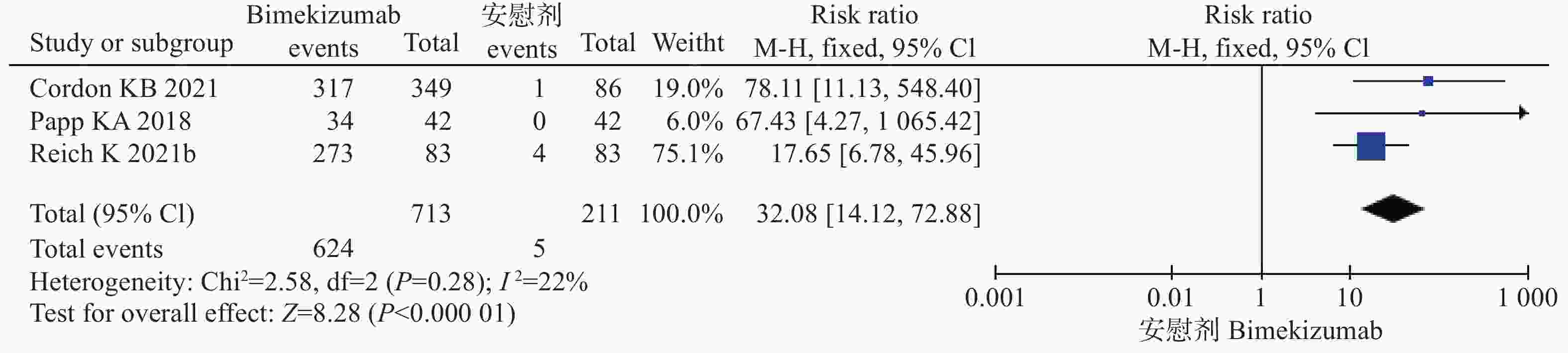
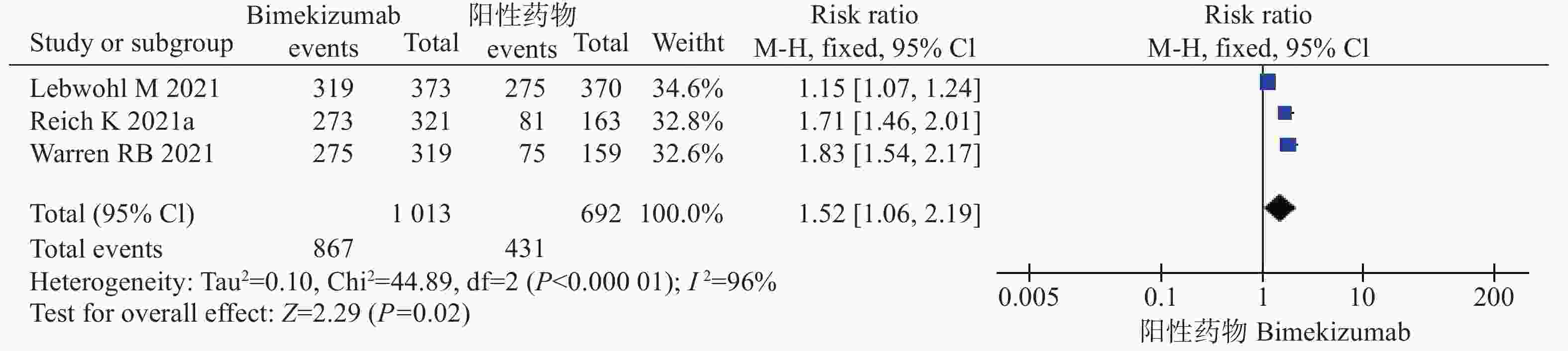
6项试验[9-13]均报道了PASI 90,其中3项研究[10-11,13]均是bim与安慰剂比较,另外3项研究[9-10,12]比较的是bim与阳性药物对PASI 90的作用。因此,将6项研究按照对照组的不同分为两组分别进行系统评价。结果显示,在bim与安慰剂对照中,各研究间不存在统计学异质性( P=0.28),采用固定效应模型进行分析。经过治疗后,bim组达到PASI 90的患者比例多于对照组,差异具有统计学意义(风险比=32.08,95%CI [14.12,72.88],P<0.00001)。在bim与阳性药物对照中,各研究间异质性存在统计学异质性( P<0.05),采用随机效应模型进行分析。经过治疗后,bim组达到PASI 90的患者比例多于阳性药物对照组,差异具有统计学意义(风险比=1.52,95%CI [1.06,2.19],P=0.02),见图4、5和表3。
结局指标 纳入研究 系统评价结果 异质性 风险比 95%CI P P I2(%) 效应模型 bim与安慰剂 PASI 90 3[10,11,13] 32.08 (14.12,72.88) <0.00001 0.28 22 固定 PASI 100 3[10,11,13] 67.62 (16.43,278.28) <0.00001 0.93 0 固定 IGA0/1 3[10,11,13] 24.19 (11.39,51.37) <0.00001 0.30 44 固定 bime与阳性药物 PASI 90 3[9-10,12] 1.52 (1.06,2.19) 0.02 <0.05 96 随机 PASI 100 3[9-10,12] 2.11 (1.22,3.66) 0.008 <0.05 97 随机 IGA0/1 3[9-10,12] 1.59 (1.00,2.53) 0.05 <0.05 94 随机 -
6项试验[9-13]均报道了PASI 100,将6项研究按照对照组的不同分为两组分别进行系统评价。结果显示,在bim与安慰剂对照中,各研究间不存在统计学异质性( P=0.93),采用固定效应模型进行分析。经过治疗后,bim组达到PASI 100的患者比例多于安慰剂组,差异具有统计学意义(风险比=67.62,95%CI [16.43,278.28],P<0.00001)。在bim与阳性药物对照中,各研究间存在统计学异质性( P<0.05),采用随机效应模型进行分析。经过治疗后,bim组达到PASI 100的患者比例多于对照组,差异具有统计学意义(风险比=2.11,95%CI [1.22,3.66],P=0.008),具体见表3。
-
6项试验[9-13]均报道了IGA评分结果,将6项研究按照对照组的不同分为两组分别进行系统评价。结果显示,在bim与安慰剂对照中,各研究间不存在统计学异质性( P=0.30),采用固定效应模型进行分析。经过治疗后,bim组达到IGA评分0或者1的患者比例多于对照组,差异具有统计学意义(风险比=24.19,95%CI [11.39,51.37],P<0.00001)。在bim与阳性药物对照中,各研究间存在统计学异质性(P<0.05),与阳性药物对比,bim组达到IGA评分0或者1的患者比例相当,差异无统计学意义(P=0.05),见表3。
-
6项试验[9-13]均报道了不良事件发生例数,将6项研究按照对照组的不同分为两组,分别进行系统评价。两组中各研究组间不存在统计学异质性(P=0.75,0.31),均采用固定效应模型进行分析。经过治疗后,与安慰剂对照,bim组不良事件发生率多于安慰剂组,差异具有统计学意义(风险比=1.38,95%CI [1.17,1.64],P=0.0002)。而阳性药物组与bim比较差异无统计学意义(P=0.06),见表4。
结局指标 纳入研究 系统评价结果 异质性 风险比 95%CI P P I2(%) 效应模型 bim与阳性药物 3[9-10,12] 1.06 (1.00,1.13) 0.06 0.75 0 固定 总不良事件 严重不良反应 3[9-10,12] 0.90 (0.55,1.45) 0.32 0.61 0 固定 上呼吸道感染 3[9-10,12] 0.92 (0.79,1.07) 0.28 0.95 0 固定 口腔念珠菌感染 3[9-10,12] 8.73 (4.80,15.84) <0.00001 0.30 16 固定 bim与安慰剂 3[10,11,13] 1.38 (1.17,1.64) 0.0002 0.31 13 固定 总不良事件 严重不良反应 3[10,11,13] 0.62 (0.22,1.80) 0.38 0.90 0 固定 上呼吸道感染 3[10,11,13] 0.73 (0.36,1.47) 0.37 0.41 0 固定 口腔念珠菌感染 3[10,11,13] 11.34 (2.11,60.86) 0.005 0.93 0 固定 鼻咽炎 3[10,11,13] 1.40 (0.79,2.48) 0.25 0.54 0 固定 -
6项试验[9-13]均报道了严重不良事件发生例数,将6项研究按照对照组的不同分为两组分别进行系统评价。两组中各研究组间不存在统计学异质性( P =0.90,0.61),均采用固定效应模型进行分析。经过治疗后,与安慰剂和阳性药物对比,bim组严重不良事件发生率差异均无统计学意义(P=0.38,0.32),见表4。
-
6项试验[9-13]报道了上呼吸道感染、口腔念珠菌感染和鼻咽炎,将6项研究按照对照组的不同分为两组分别进行系统评价。两组中各研究组间不存在统计学异质性( P>0.05),均采用固定效应模型进行分析。经过治疗后,与安慰剂和阳性药物对照,上呼吸道感染和鼻咽炎差异均无统计学意义(P>0.05)。但是bim组的口腔念珠菌感染的发生率多于安慰剂组,也多于阳性药物组(与安慰剂对比:风险比=11.34,95%CI [2.11,60.86],P=0.005), 与阳性药物对比:风险比=8.73,95%CI [4.80,15.84],P<0.00001),见表4。
-
对bim与阳性药物对照的有效性指标(异质性较大)进行敏感性分析,去除Lebwohl[12]研究,结果变化见表5,IGA评分0或1的患者比例有所改变,由与对照组相比无统计学差异变为优于对照组,其他结果无变化(试验组优于对照组),去除权重大的研究并未改变系统评价得到的结论。
指标 剔除前 剔除后 风险比 95%CI P 风险比 95%CI P PASI 90 1.52 (1.06,2.19) 0.02 1.77 (1.57,1.98) <0.00001 PASI 100 2.11 (1.22,3.66) 0.008 2.66 (2.15,3.30) <0.00001 IGA 0或1 1.59 (1.00,2.53) 0.05 1.96 (1.06,3.62) 0.03 -
银屑病作为一种系统性免疫炎症皮肤疾病,机制不明,难以治愈。银屑病发生过程中T细胞过度活化,其中,Th17细胞可特异性表达IL-17A和IL-17F引起炎症反应,bim可同时作用与IL-17A和IL-17F,发挥抗炎作用抑制银屑病的发展[14]。bim作为首个双重靶点抑制剂,临床研究中展现了良好的疗效和安全性。为了进一步分析bim的疗效,本次研究对bim的临床研究进行系统评价。结果显示,经过治疗后,bim组达到PASI 90,PASI 100和IGA评分达到0或1的患者比例均多于安慰剂组,提示bim对中重度的斑块状银屑病的疗效远优于安慰剂,疗效确切。同时与阳性药物对比,bim组达到PASI 90,PASI 100的患者多于对照组,IGA评分达到0或1的患者比例则无统计学差异,提示bim治疗中重度斑块状银屑病的疗效优于阿达木单抗、乌司奴单抗和司库奇尤单抗。出现此结果的可能原因,阿达木单抗通过作用于TNF发挥作用[15],乌司奴单抗通过抑制IL-12/23[16],司库奇尤单抗通过抑制IL-17A发挥作用[17],bim则是通过抑制双靶点IL-17A和IL-17F发挥作用,这种双靶点作用机制使得bim表现出更为强大的疗效,但系统评价结果中的IGA评分达到0或1的患者比例仅显示疗效相当,因此还需更多的与阳性药物对比的临床试验来证实结论。值得注意的是,在进行系统评价过程中,研究的异质性较高,可能与3项研究分别使用乌司奴单抗、阿达木单抗和司库奇尤单抗作为阳性对照有关,将异质性高的指标进行敏感性分析,试验组IGA评分达到0或1的患者比例优于阳性药物组,但并未改变本次系统评价得到的结论。
安全性方面结果显示,bim的总不良反应事件的发生率多于安慰剂,与阳性药物相当。在严重不良反应事件发生率上,bim与安慰剂和阳性药物对比无统计学差异。在导致上呼吸道感染和鼻咽炎方面,bim与安慰剂和阳性药物对比无统计学差异。但在导致口腔念珠菌感染方面,bim的发生率高于安慰剂组,也高于阳性药物对照组,提示bim的安全性良好,但口腔念珠菌感染率较高。有研究显示针对IL-17靶点的生物制剂会导致口腔念珠菌的感染率提高[18],而bim正是通过双重抑制IL-17发挥作用,其口腔念珠菌感染率确实相较于其他药物也有所提高,侧面印证本次研究结果。有综述认为IL-17的拮抗剂在严格监测下使用还是较为安全,严重不良反应罕见[19]。针对bim引起的念珠菌感染,使用过程中定期监测念珠菌发生的口腔感染,一般不良反应轻微,也可进行抗念珠菌治疗来保障患者的用药安全。
本研究的局限性:①纳入文献的语种限定为中文和英文,可能存在发表偏倚。②本次纳入的与阳性药物对照的研究不多,还需更多大样本,多中心的临床研究来进一步证实本次研究得到的结论。
综上所述,bim在治疗中重度斑块状银屑病的疗效显著,不良反应轻微可耐受,但临床使用过程中要注意口腔念珠菌的感染。
Efficacy and safety of bimekizumab in treatment of moderate/severe plaque psoriasis: a systematic review
doi: 10.12206/j.issn.2097-2024.202203089
- Received Date: 2022-03-21
- Rev Recd Date: 2022-09-01
- Available Online: 2023-07-14
- Publish Date: 2023-07-25
-
Key words:
- Bimekizumab /
- psoriasis /
- efficacy /
- safety /
- systematic review
Abstract:
| Citation: | WEI Xun, GAO Shan. Efficacy and safety of bimekizumab in treatment of moderate/severe plaque psoriasis: a systematic review[J]. Journal of Pharmaceutical Practice and Service, 2023, 41(7): 449-454. doi: 10.12206/j.issn.2097-2024.202203089 |








 DownLoad:
DownLoad: