-
药用植物中的次生代谢物是中药药效物质的主要来源,已知的植物次生代谢物生物合成途径有乙酸-丙二酸途径、异戊二烯途径、莽草酸途径等[1],探究植物生物合成的调控因素不仅能提升药材的品质,也为中药有效成分体外合成的工业化提供可能。
植物昼夜节律钟是植物体内应对光照、温度等外界因素随昼夜节律性改变而进化出的一套适应机制[2],对植物生长发育具有不可或缺的作用。大量研究表明,如黄酮类化合物合成的相关结构基因表达,也具有明显的昼夜节律性特点,受昼夜节律钟调控[3-4]。昼夜节律钟的核心部分中央振荡器是MYB蛋白LHY(late elongated hypocotyl)、CCA1(circadian clock associated 1)和伪应答调控蛋白家族(PRRs,pseudo-response regulators)组成,对维持植物昼夜节律的稳定至关重要[5-6]。
PRRs基因都带有2个保守的结构域,氨基端的响应接受结构域(receiver-like domain,RLD),其结构上与磷酸接受域相似,羧基端带有的CCT(Constans/Constans-like/TOC1)结构域,这2个结构域被一个保守程度不高的“可变域”所分隔[7-9]。目前研究发现在CO、CO-like以及TOC1基因中也有带此类结构域,对于植物开花进程有着重要作用[10-11]。
研究表明PRRs家族基因具有增加植物抗逆性,影响植物生物量的积累[12-14],以及调控花发育及衰老等作用[15]。目前对模式植物中PRRs基因的研究较多,如在拟南芥以及水稻中的PRRs基因证明具有调控开花周期的作用[17],但药用植物中PRRs基因的研究则罕见报道。
中药红花(Carthami flos)是菊科植物红花(Carthamus tinctorius L.)的干燥花,有活血化瘀的功效。研究表明,红花主要药效物质为黄酮类化合物,如羟基红花黄色素A(HSYA)、红花素、槲皮素、山奈酚、野黄芩苷[18]等,目前已有对红花黄酮类化合物生物合成的关键基因查尔酮合酶、查尔酮异构酶、糖基转移酶等多种研究[19-20],但调控红花中黄酮类化合物生物合成途径的基因未完全明确。验证昼夜节律钟调控红花中黄酮类化合物的生物合成对提升红花品质意义重大。
本研究依据前期红花转录组数据库基因注释筛选昼夜节律相关基因,并与红花黄酮类化合物的积累量进行相关分析,得到具有调控红花黄酮类化合物生物合成功能的昼夜节律基因,通过qPCR、液质联用(UHPLC-MS)等方法以期阐释PRRs基因的特征与功能,为进一步研究昼夜节律钟调控红花黄酮类化合物的生物合成积累资料。
HTML
-
植物材料:云南巍山红花品系(编号ZHH0119),种植于海军军医大学药学院温室,温室条件:恒温25 ℃,昼夜节律为16 h光照/8 h黑暗。仪器与试剂:荧光qPCR仪:ABI7500;Phanta Max Master Mix高保真酶,Trans Top green qPCR super mix,Trans one-step cDNA synthesis super mix逆转录试剂盒(北京全式金公司);Meitler Toledo电子天平(十万分之一量程);高效液相色谱仪:Agilent1290 Infinty LC system; 质谱仪:Agilent 6538 Accurate Mass。
-
取用新鲜红花的花冠,根、茎、叶约100 mg研磨成粉。依据Plant Zol说明书提取总RNA,并用紫外分光光度计测定总RNA浓度与质量,样品的A260/A280在1.9~2.1之内可认为符合后续实验要求。将其作为模板逆转录合成cDNA第一链,−20 ℃保存备用。
-
基于红花转录组数据库,结合基因注释筛选出昼夜节律相关基因,通过红花花冠表达谱获取表达量,与红花代谢组数据库中不同花期黄酮类化合物的积累量进行Pearson分析,获取与黄酮类化合物积累量相关系数r≥0.7的昼夜节律基因进行生物信息学分析,设计引物(表1)进行克隆。PCR产物进行凝胶电泳,回收含有目的条带的凝胶,连接载体后转化大肠杆菌感受态细胞,LBA平板培养,挑取阳性克隆送至上海生工生物工程有限公司测序。
引物名称 引物序列 PRR1-F ACCTCAAGGGCCACTGGTTC PRR1-R GTAACAAAAGACTTTCTGAA -
在NCBI网站用BLAST在线分析红花PRR1全长序列以及编码蛋白的氨基酸序列进行比对以及同源性分析;在ExPASy在线工具SOMPA得出所编码蛋白的二级结构特征;通过Swiss-Model同源建模预测蛋白三级结构;在ClustalX 2.1软件对其编码蛋白的氨基酸序列与同源蛋白的氨基酸序列进行多重比对分析;使用相邻节点算法(Neighbor-Joining)构建系统进化树,自展分析法(Bootstrap analysis)进行1 000次重复验证进化树可靠性。
-
以红花根、茎、叶、花4个部位;花冠开花前3 d(Ⅰ期)、开花1 d(Ⅱ期)、开花3 d(Ⅲ期)、开花5 d(Ⅳ期)4个时期[12]以及1 d中8个时间点(6:00、9:00、12:00、15:00、18:00、21:00、0:00、3:00)的花冠第一链cDNA为模板,设计RT-qPCR引物,以Ct60s(KJ634810)作为内参基因,进行qPCR实验,每个样品设3个复孔。
-
取红花Ⅲ期单日内4个时间点(9:00、12:00、15:00、21:00)的花冠烘干至恒重,精密称取5.00 mg置1.5 ml离心管,再加入精密量取的1 ml 60%甲醇,室温放置12 h后超声处理40 min,12 000 r/min,10 min离心取上清液,UHPLC-MS在正、负离子模式下进行检测(表2),参比离子:正离子模式为121.050 9,922.009 8;负离子模式为119.036 3,966.000 7,数据采集与分析使用Agilent MassHunter Analysis4.0软件。以柚皮素、芹菜素、槲皮素、HSYA、山奈酚、红花素、山奈酚-3-O-葡萄糖苷以及野黄芩素为对照品。
色谱条件 质谱条件 色谱柱:Agilent ZORBAX C18(3.5 μm,2.1 mm ×100 mm) 毛细管电压:3.5 kV 流动相:A:0.1%甲酸-水,B:乙腈 锥孔电压:60 V 流速:0.4 ml/min 离子源温度:350 ℃ 柱温:40 ℃ 碎裂电压:120 V 进样量:0.4 ml 采集范围:50~1 100 m/z 梯度洗脱:0 min,5%B; 4 min,20%B;
6 min, 21% B; 9 min, 26% B; 11 min, 40% B; 15 min, 80% B; 17 min, 95% B -
使用STRING数据库对CtPRR1基因进行蛋白互作网络分析,可信区间设置为0.4。利用Python下的networkX将互作基因进行可视化。
-
将红花cDNA均一化处理得到红花酵母双杂cDNA文库,与载体PGADT7进行同源克隆,产物转化大肠杆菌感受态细胞,涂布LBA平板,37 ℃培养过夜,挑取单克隆菌落进行菌液PCR验证
-
根据PRR1 ORF设计同源引物引入BamHI、XhoI酶切位点。PCR产物经电泳后回收,连接酶切载体pGBKT7转入大肠杆菌,测序验证后完成pGBKT7-PRR1 bait载体的构建。
将pGBKT7-PRR1bait质粒通过PEG/LiAc法转化酵母感受态细胞,涂布SD平板,28 ℃培养,挑取单克隆进行菌液PCR鉴定。将阳性单克隆酵母菌液划线涂布含有X-α-gal和Aba的平板。
-
将酵母感受态细胞、载体DNA、红花酵母双杂cDNA文库质粒按共转法混合处理后均匀涂布于SD/-His/-Trp/-Ura三缺平板培养,挑取单克隆转移至含有X-α-gal的SD/-His/-Trp/-Ura培养基,扩增阳性质粒用于测序以及酵母双杂验证。
-
实验结果经SPSS19.0软件处理,计量资料统一表示为(
${{\bar x}} \pm {{s}}$ ),组间比较采用ANOVA分析,以P<0.05为差异具有统计学意义。
1.1. 材料与仪器
1.2. 红花总RNA的提取与cDNA第一链的合成
1.3. 红花PRRs基因的筛选与克隆
1.4. 红花PRR1生物信息学分析
1.5. 红花PRR1基因表达分布特征分析
1.6. 红花中黄酮类化合物含量测定
1.7. 红花PRR1蛋白互作体系研究
1.7.1. 红花PRR1蛋白互作网络预测
1.7.2. 红花酵母双杂cDNA文库构建
1.7.3. 红花PRR1载体构建与酵母转化
1.7.4. 酵母双杂文库筛选红花PRR1互作蛋白
1.8. 统计分析
-
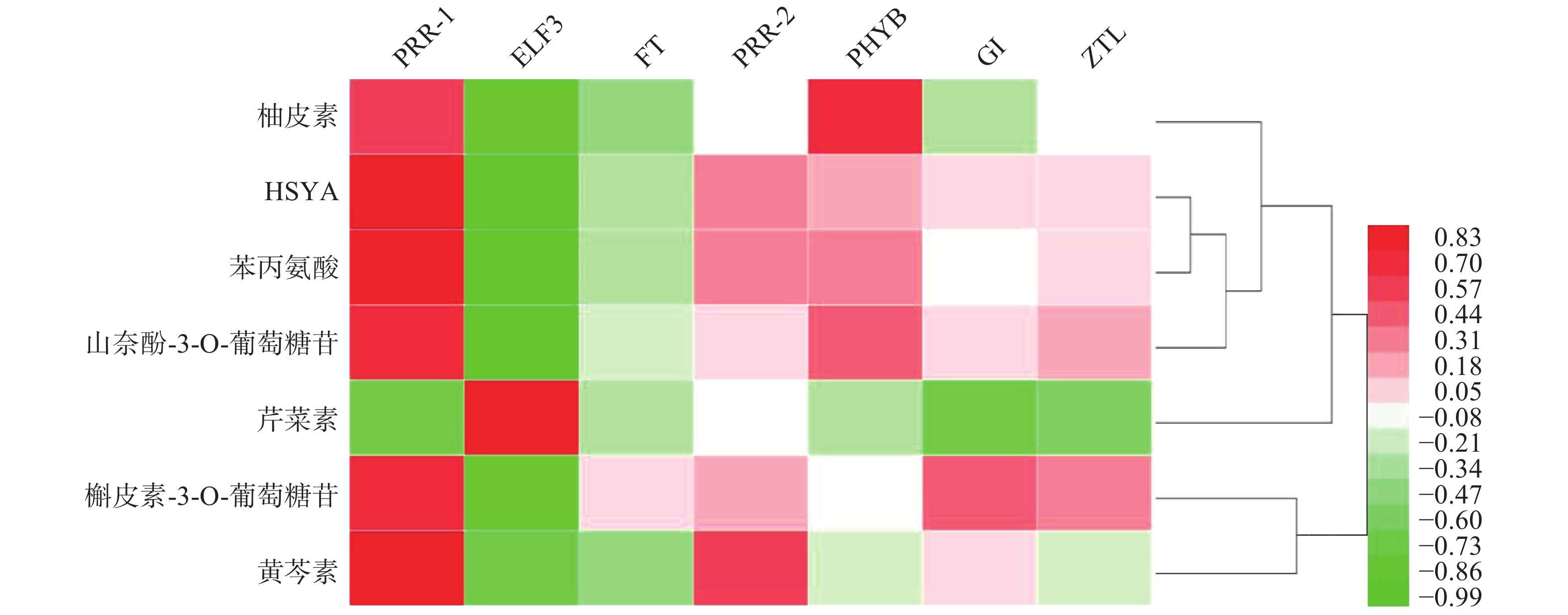
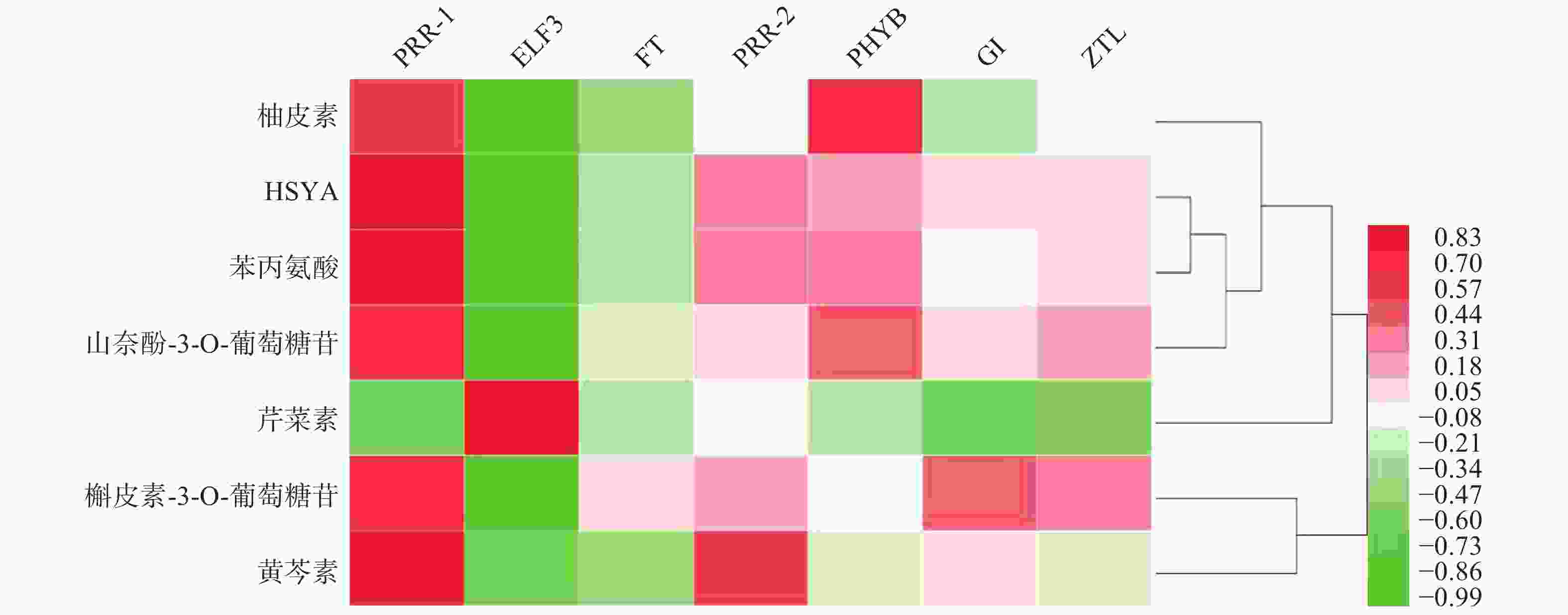
基于红花花冠转录组数据库的基因注释,检索出PRR1、PRR2、ELF3、FT、PHYB、GI、ZTL7个昼夜节律基因,将其在花冠不同时期的表达量与红花代谢组数据库中柚皮素、HYSA、苯丙氨酸、山奈酚-3-O-葡萄糖苷、芹菜素、槲皮苷、野黄芩素、槲皮素-3-葡萄糖苷7个化合物含量进行PEARSON相关性分析,如图1所示,PRR1与红花中主要黄酮类成分的积累量具有良好的相关性(r≥0.7)。
-
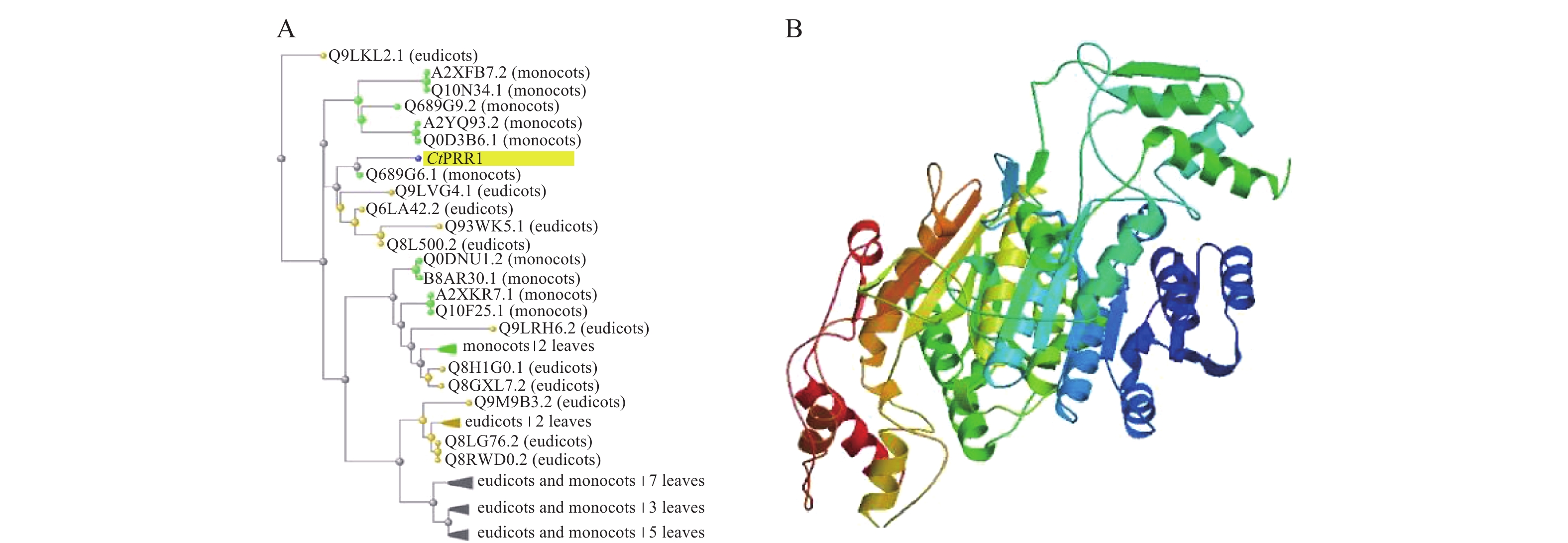
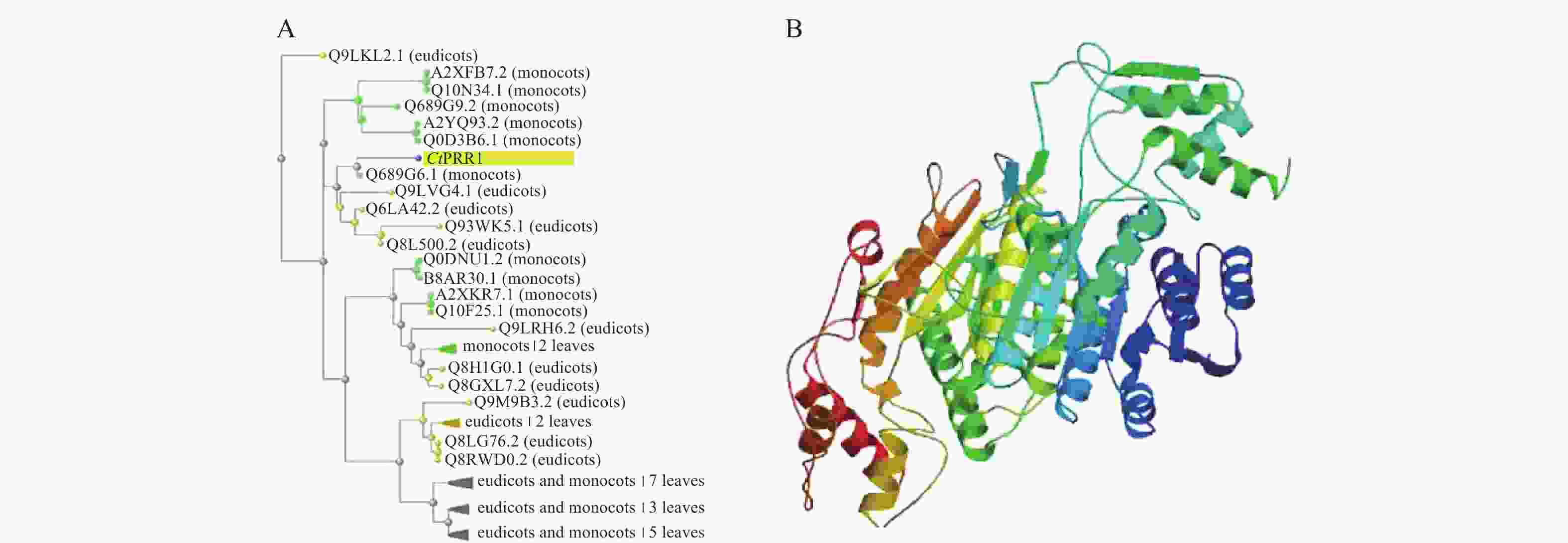
在红花全长转录组数据库中得到的PRR1基因全长序列3 201 bp,ORF FINDER结果显示开放阅读框1 549~2 814 bp,编码421个氨基酸,命名为CtPRR1(GenBank登录号:MW492035),将全长序列进行BLAST,系统发育进化树分析如图2A,CtPRR1氨基酸序列与水稻(Oryza sativa L.)OsPRR73氨基酸序列(A2XFB7.2)同源性最高。Prot-param分析PRR1基因所编码的蛋白质分子式C1900H3039N611O653S15,分子量为45 300,理论pI=8.52,对PRR蛋白质三维结构预测如图2B,Prot Scale分析表明预测PRR1蛋白为亲水性蛋白,无信号肽属非分泌蛋白;蛋白跨膜性分析预测PRR不含有跨膜区域,为非跨膜蛋白。
-
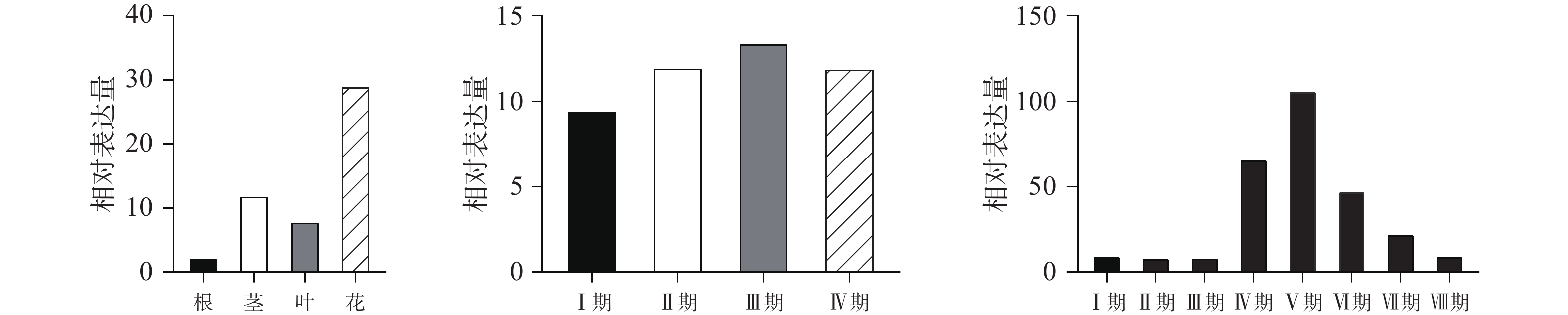
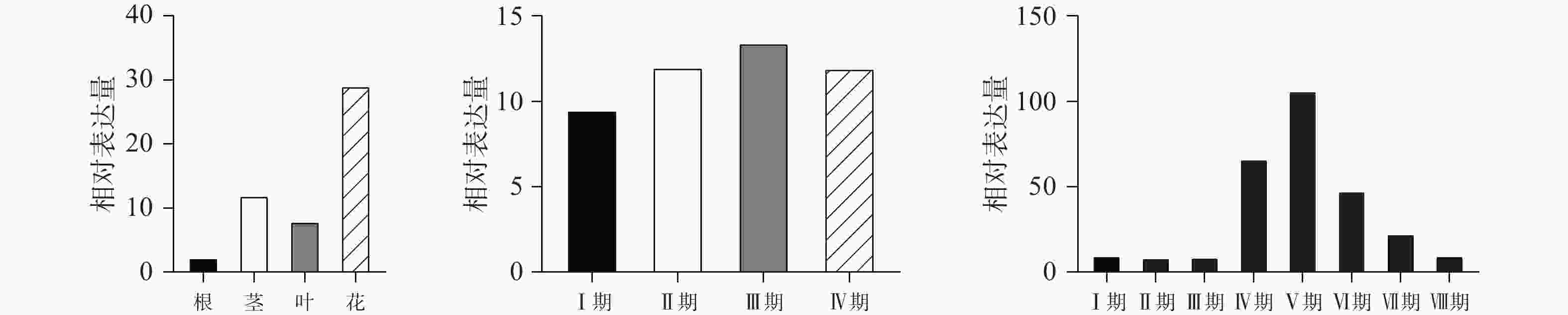
qPCR结果表明(图3A)在红花不同部位中,CtPRR1基因在花中的表达量最高,且与根、茎、叶都有显著性差异(P<0.05),对红花花冠Ⅰ期、Ⅱ期、Ⅲ期、Ⅳ期的CtPRR1基因的表达情况进行分析,CtPRR1在Ⅰ期花冠中表达含量最低;Ⅱ期表达水平略有上升,与Ⅰ期无显著性差异;Ⅲ期花冠中表达量明显上升,相比Ⅰ,Ⅱ期具有显著性差异,Ⅳ期花冠中的CtPRR1基因表达水平略微下降(图3B),表明CtPRR1基因在Ⅲ期花冠中转录水平最高,CtPRR1在不同时间表达量的变化与红花黄酮类化合物积累量的变化相符[22]。对红花8个时间点的花冠CtPRR1表达量分析发现CtPRR1表达量在日间6:00至18:00逐渐升高,18:00达峰值,晚间21:00至2:00逐渐下降,3:00最低,表达水平在白天与夜晚两个连续的时间周期内呈现昼夜节律性(图3C)。
-
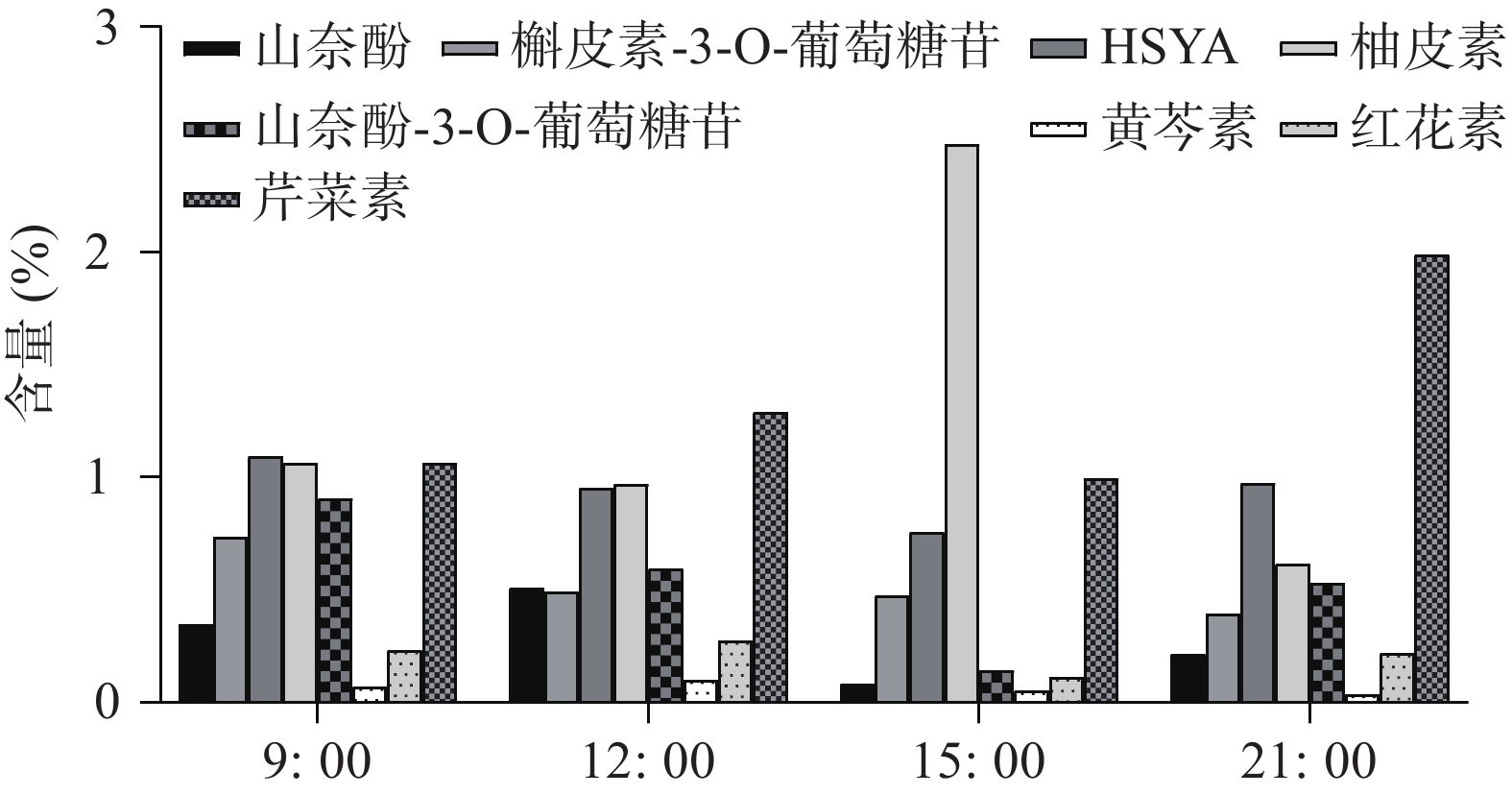
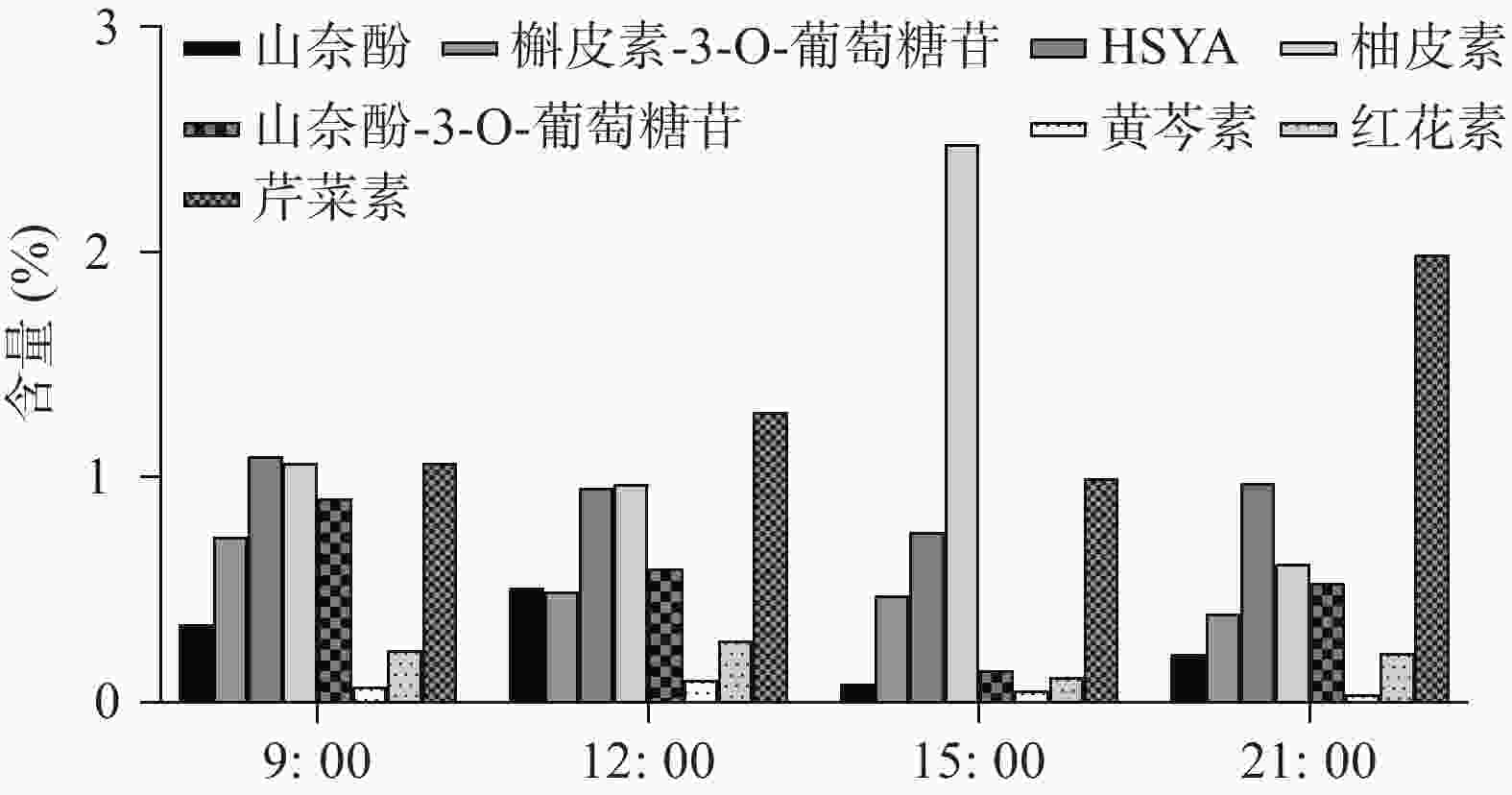
UHPLC-MS检测黄酮类化合物在单日内不同时间的含量变化(图4),除柚皮素外的7个化合物在白天含量逐渐降低,而在晚间含量又升至较高的水平,柚皮素则相反在白天升高,晚间下降,但8个化合物含量变化也呈现昼夜节律性,与同时间点CtPRR1的表达量进行PEARSON分析得到红花素(r=−0.9485)、山奈酚(r=−0.9423)、野黄芩苷(r=−0.9504)、HSYA(r=−0.8372)、山奈酚-3-O-葡萄糖苷(r=−0.8792)、柚皮素(r=0.7415)、芹菜素(r=−0.6652)、槲皮素(r=−0.4876),目前研究认为柚皮素在红花黄酮类化合物生物合成途径的上游[20],而CtPRR1与柚皮素呈正相关,与其他化合物呈负相关,说明CtPRR1对整体黄酮类化合物生物合成具有负调控作用而导致柚皮素的积累量增多,进一步说明CtPRR1参与调控红花黄酮类化合物的合成。
-
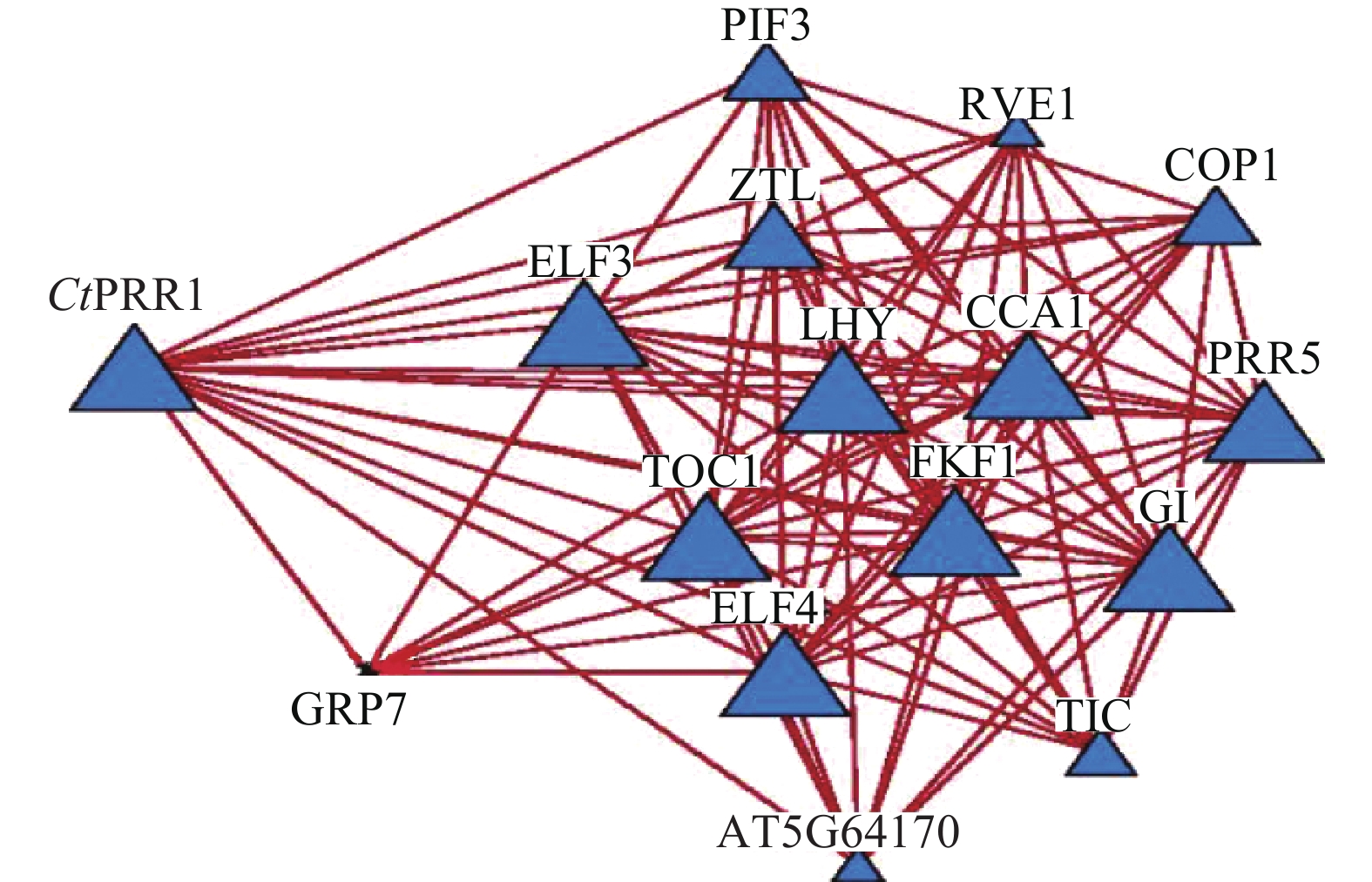
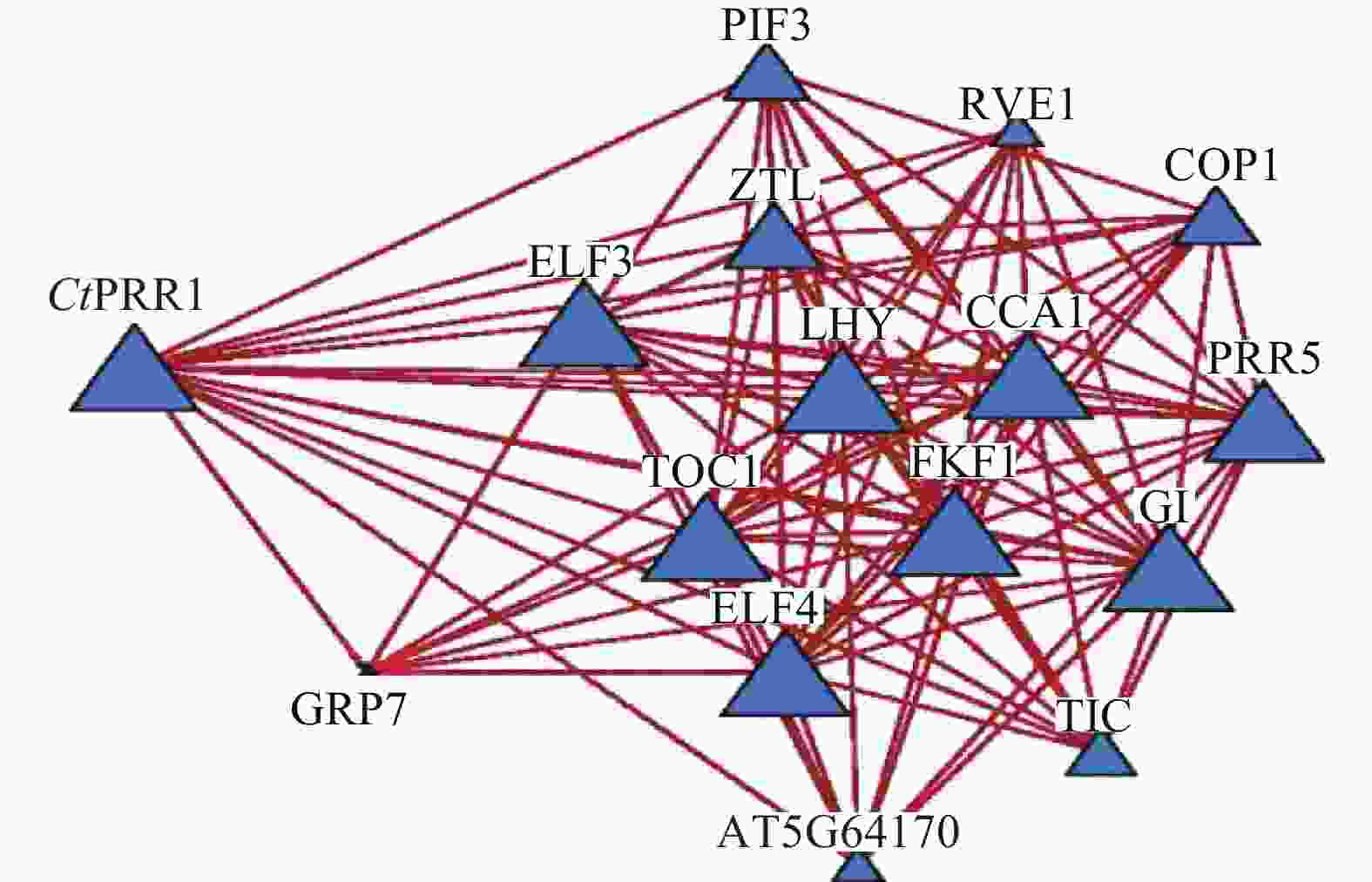
STRING数据库预测红花转录组数据库中CtPRR1的互作蛋白,获得互作蛋白TOC1、PIF3、COP1、ZTL、LHY、ELF4、ELF3、CCA1、GI、PRR5、GRP7、TIC、FKF1、RVE114个,互作关系网络如图5。与PRRs基因共同参与调控植物生长发育,调控植物次生代谢途径。由此获得了较为完善的红花昼夜节律核心元件系统,为进一步探索昼夜节律调控红花次生代谢的分子机制提供了依据。
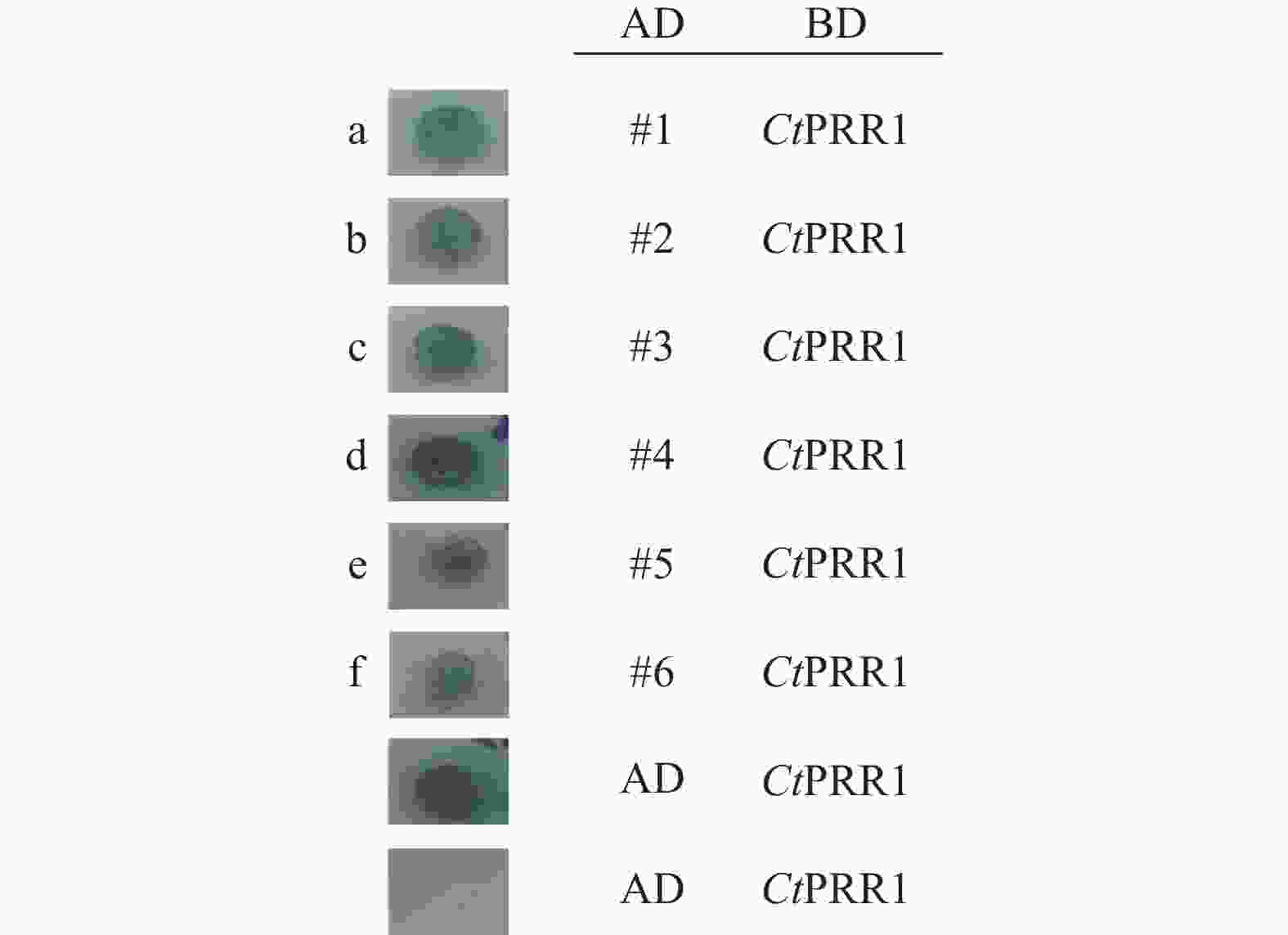
通过酵母双杂实验发现,转入pGBKT7-PRR bait质粒的酵母细胞在28 ℃生长4 d后情况正常。带有pGBKT7-PRR bait载体的酵母细胞与构建的红花cDNA文库质粒共转后,28 ℃培养2 d后可以观察到蓝色菌斑出现,4 d后出现直径约2 mm的蓝色单克隆菌斑(图6),菌液PCR鉴定为阳性克隆。结果如表3所示,有2个热休克蛋白,3个AP2转录因子,热休克蛋白具有增强植物抗逆性的功能,AP2转录因子广泛参与植物生长发育,调控体内次生代谢。
序号 蛋白家族名称 预测功能 1 热休克蛋白 广泛参与植物响应外界环境胁迫,生物合成以及生长发育相关的转录调控 2 热休克蛋白 3 AP2转录因子 4 AP2转录因子 5 AP2转录因子
2.1. 红花昼夜节律相关基因的筛选
2.2. 红花PRR1基因全长克隆与生物信息学分析
2.3. CtPRR1基因在红花中的表达特征
2.4. 红花中黄酮类化合物含量测定
2.5. CtPRR1蛋白互作研究
-
红花作为常用的活血化瘀中药,对其主要药效物质黄酮类化合物的生物合成途径及调控机制的研究越来越多[20],但目前红花黄酮类化合物生物合成途径及调控机制仍未阐明。
本研究首次克隆了一个PRRs家族基因CtPRR1,生物信息学分析表明其与水稻、拟南芥等其他物种中的PRRs家族基因序列高度相关,说明红花中的PRRs基因具有高度保守性。CtPRR1基因主要在花中表达且开花后第3天时表达量最高,与红花不同花期黄酮类化合物的累积规律一致,存在显著相关。我们认为,CtPRR1调控了红花黄酮类化合物的生物合成。进一步的研究发现,CtPRR1的单日表达量在日间逐渐升高,晚间逐渐下降;随着CtPRR1在单日表达量的升高,芹菜素、槲皮素、HSYA、山奈酚、红花素、山奈酚-3-O-葡萄糖苷以及野黄芩素积累量为白天逐渐降低,晚间逐渐升高。CtPRR1对红花这些黄酮类成分的昼夜节律性积累积起负调节作用;唯CtPRR1与柚皮素的积累量呈正相关,可能与柚皮素处于黄酮生物合成途径的较上游以及参与其他代谢过程并受到其他调控基因的影响有关。
PRRs与CCA1、LHY基因作为昼夜节律系统中的核心元件,对多种植物的昼夜节律钟输出途径中与黄酮合成结构酶基因具有相互作用[22-23],本研究发现红花CtPRR1可能受2个热休克蛋白,3个AP2转录因子的影响对黄酮化合物的积累起负调节作用,丰富了昼夜节律基因调控黄酮类化合物机制的研究资料。
本研究结果为深入研究红花昼夜节律基因对黄酮生物合成途径的调控机制提供了资料。下一步的工作,我们将采用基因过表达以及基因敲除技术结合代谢物分析,进一步验证CtPRR1调控红花黄酮类化合物生物合成的功能及调控网络,为阐明CtPRR1的功能提供重要依据。








 DownLoad:
DownLoad: